⑧輸血副作用
- 輸血副作用は,赤血球を主体とした溶血性,それ以外の白血球,血小板,血漿タンパクなどが主な原因となる非溶血性に分類されるが,溶血性をさらに副作用発症までの時間で分類した場合は,発症時間が24時間以内を急性溶血性輸血副作用(AHTR)とし,24時間以降を遅発性溶血性副作用(DHTR)として区別している。
- このセクションでは,主な輸血副作用について紹介する。
- 溶血性輸血副作用は免疫学的な原因により発生し,輸血後24 時間以内の発生か否かにより,急性溶血性輸血副作用と遅発性溶血性輸血副作用に分類される(表1)。
- 非溶血性輸血副作用は,輸血副作用の中で最も多く,副作用の要因から免疫学的要因と非免疫学的要因に分けられる。免疫学的要因には,発熱反応(発熱,悪寒戦慄など),アレルギー反応(蕁麻疹,掻痒感など),輸血関連肺障害(TRALI),輸血後紫斑病(PTP),輸血後移植片宿主病(PT-GVHD)があり,非免疫学的要因には,輸血後関連循環過負荷(TACO),細菌感染症,輸血後感染症がある。
- 免疫反応は,異物(抗原)を排除するために働く生体にとって不可欠な生理機能であるが,時に特定の抗原に対して過剰な反応を示すことがあります。この過剰反応(蕁麻疹,掻痒感,呼吸困難,血圧低下等)をアレルギー反応といい,特に反応が強く,呼吸器・心血管系の症状を伴い血圧低下や意識障害をきたす様な全身性のものをアナフィラキシーと呼ばれています。重篤なアナフィラキシーが起こることはまれであるが,アレルギー反応は輸血副作用のなかではもっとも頻度が高い副作用です。
- 輸血によるアレルギーの原因として特定されているのは,血漿蛋白(IgAやハプトグロビン)欠損患者で過去の輸血等により当該蛋白に対する抗体が産生されている場合のみであり,原因のほとんどは解明されていません。原因物質として特定されてはいませんが,食物アレルギーのある患者に,献血前に当該食物を摂食した献血者の血液を輸血してアレルギーが発生したとの報告があります。
- 対策として,赤血球製剤や血小板製剤の輸血によってアナフィラキシーを繰り返す患者には,洗浄赤血球や洗浄血小板等が有用である。アレルギーの原因が血漿蛋白欠損と特定されている患者に血漿製剤を輸血する際は,当該血漿蛋白欠損の献血者由来の血漿製剤が必要となる場合があるので,血液センターに相談する。抗ヒスタミン剤やステロイドの事前投与には明確なエビデンスはありませんが,予防投与を行う場合には輸血の30~60分前に実施します。
- 輸血後6時間以内に,非心原性の急激な肺水腫による呼吸困難を呈する重篤な副作用である。現在,輸血関連死の主な原因の一つとなっている。
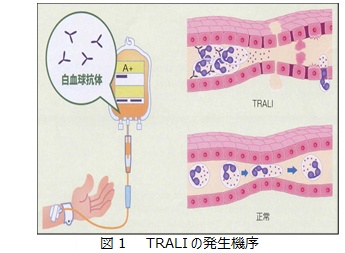
- 発症のメカニズムは,血液製剤中の白血球抗体(HLA抗体,好中球抗体)やその他の未確認物質と患者白血球や肺毛細血管内皮細胞との抗原抗体反応により,好中球が活性化され、肺の毛細血管に損傷を与えることで起こる(図1)。
- 発生頻度であるが,日本赤十字社の報告によると2004年~2011年の間299例の報告があり,17例が死亡している。8万~22万パックに1例の頻度であり,血小板製剤による事例が多い。
- 診断基準については,従来,TRALIとpossible TRALIに分類されていたが,2019年に英国SHOTによりタイプⅠとⅡに再定義された(表2)
- 治療に関しては,まず早期に診断することが重要となってくる。輸血開始後に急激な呼吸障害が現れた場合には,直ちに輸血を中止(ラインは確保)し,呼吸管理を行う必要があります。早期の確定診断には,胸部X線,中心静脈圧,胸部聴診,バイタル,血液ガスなどが有効です。重篤な場合,人工呼吸器の装着などが必要になります。
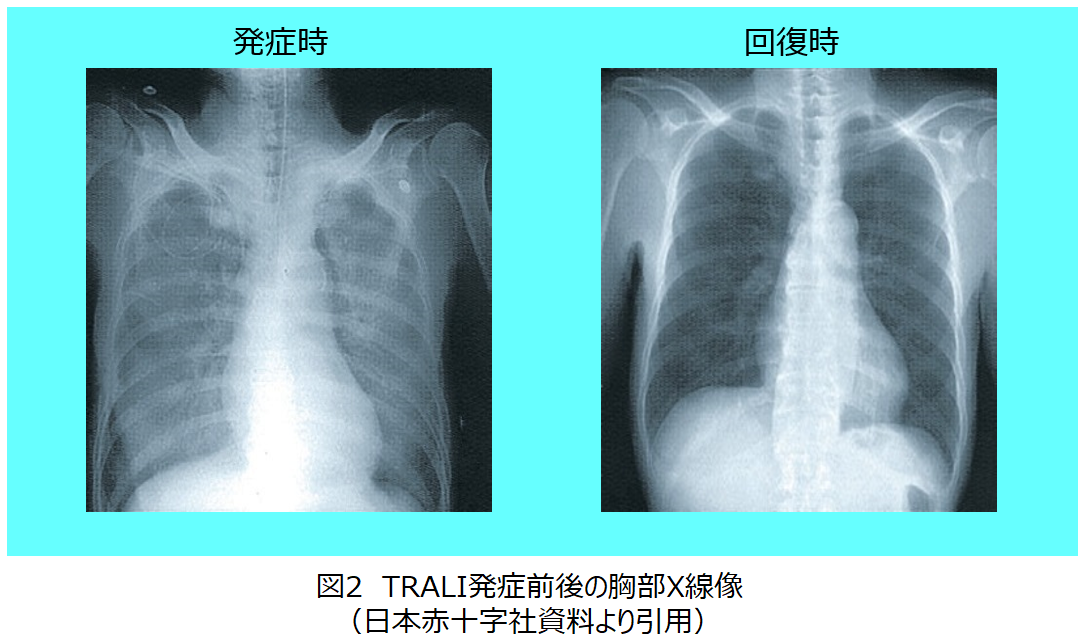
TRALI発症前後の胸部X線像を示します(図2)。 - TRALIの予防に関しては,妊娠により女性血液中につくられた抗体が原因になっていることが外国での取り組みから明らかであることから,わが国でも2012年から400mL由来のFFPの製造を男性由来のみとしており,FFPによるTRALIの発生は減少してきた。発生原因に関して,白血球抗体や血漿抗体以外の未確認物質による可能性があるため,輸血中・輸血後に十分観察を行い,呼吸器症状がでた場合はTRALIを念頭に置き対処する必要がある。
- 製剤中の血小板抗原(HPA)に対する患者の抗体により,輸血後5日から12日後に発症する血小板減少症で,HLA抗体が原因となる血小板輸血不応と異なり,患者自身の血小板も急激に減少し,出血傾向(粘膜出血,血尿,全身多発性出血斑等)を呈することが特徴である。妊娠や輸血で感作を受けている患者に起こり,主にHPA-1a抗原に対する抗体が関与していると考えられていますが,その他の抗原の関与も示唆されています。患者の血小板が破壊される機序ははっきりしていません。治療としては,IVIGやステロイドの大量投与,血漿交換等が行われます。
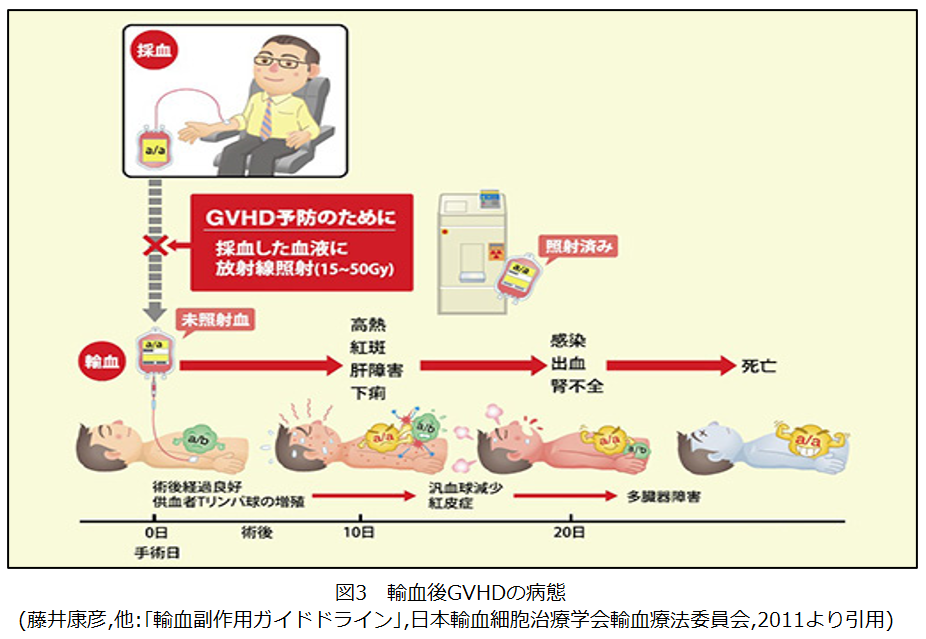
- 輸血後GVHDは,輸血用血液製剤中の供血者リンパ球が生着し,患者の体組織を攻撃・傷害することによって起きる病態です(図3)。輸血後1~2週間で発熱・紅斑が出現し,肝障害・下痢・下血等の症状を伴うとともに,骨髄無形成・汎血球減少症,多臓器不全を呈して,ほとんどの症例で輸血から1カ月以内に致死的経過をたどります。
- 輸血後GVHDに関して,有効な治療法はないので,輸血用血液に放射線照射をして予防することが重要となります。わが国では,1998年からFFPを除く全ての血液製剤に放射線照射が実施され対策が取られており,2000年以降,放射線照射血液製剤による輸血後GVHDは報告されていません。
- また,院内採取した同種血の使用に関しては,輸血後GVHD回避のためにも極力避けるべきである。少なくとも,未照射地を輸血してはならない。
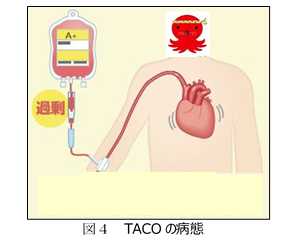
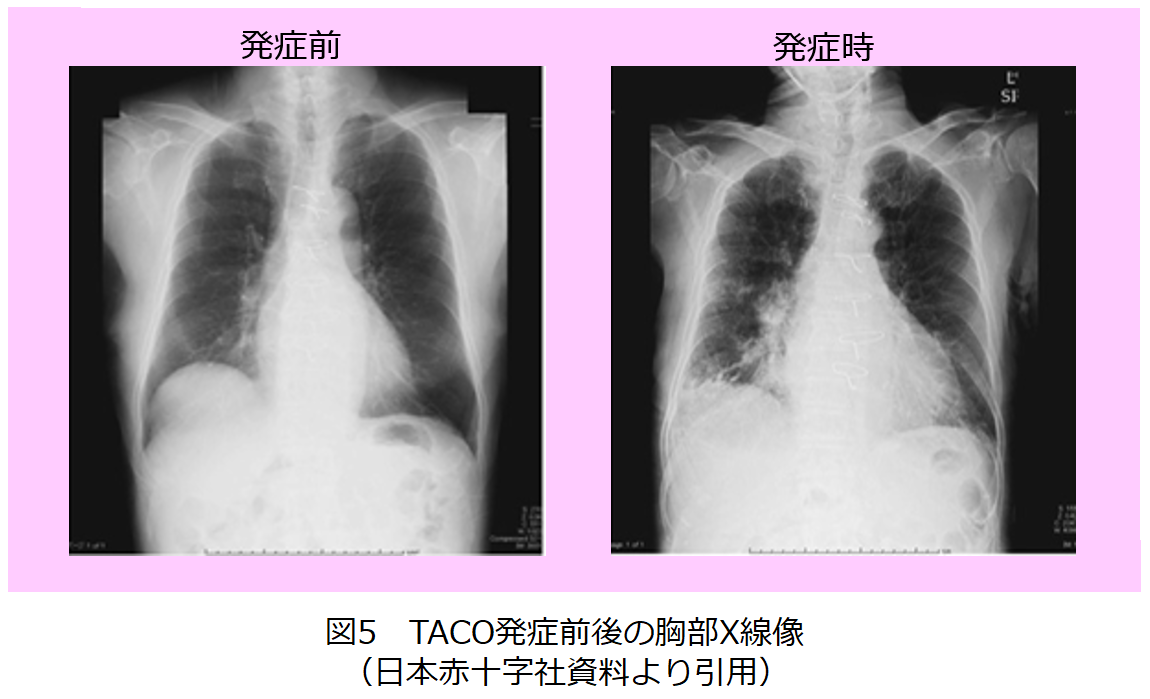
- TACOとは,輸血に伴う循環負荷による心不全(図4)であり,呼吸困難,頻脈,血圧上昇などを認める。胸部X線でうっ血性の心不全の所見(図5)を認めることがあり,輸血後6時間以内の発症が多い。
- 症状としては,呼吸困難,起座呼吸,うっ血性心不全,チア
ノ-ゼ,頻脈,血圧上昇がみられ,補助診断として,BNP, NT-pro BNP,心エコーが有効である。基本的な病態は心不全であり,日本赤十字社における評価基準を表3に示す。確定診断は容易ではなく,虚血性心疾患が存在する場合はTACOとは診断しない。典型的なTRALIとTACOの特徴を表4に示す。 - TACOの発生頻度は,日本赤十字社の報告によると,2016年では33件報告されており,年々増加しています。欧米含め,TACOはABO不適合輸血,TRALIと合わせて,重篤な輸血後関連副作用といわれています。
- TACOはどの年齢層でも発症がみられるが,特に高齢者に多く,赤血球輸血が原因の場合が多い。特に心毒性や慢性貧血などの心機能障害や,腎機能障害をもった患者や,低アルブミン血症,高齢者(特に70歳以上),低体重患者に輸血する場合は,輸血量や速度に注意し,十分観察する必要がある。
- 血液製剤によるウイルス感染については,献血血液へのHBc抗体や個別NATの導入により,感染血液の多くが排除されるようになった。一方で,血液製剤に混入した細菌汚染による輸血後感染症のリスクも存在しており,致死的な合併症となることから,注意する必要がある。日本赤十字社の報告では,1998年~2008年の11年間に366例の輸血後細菌感染疑いが報告されている。
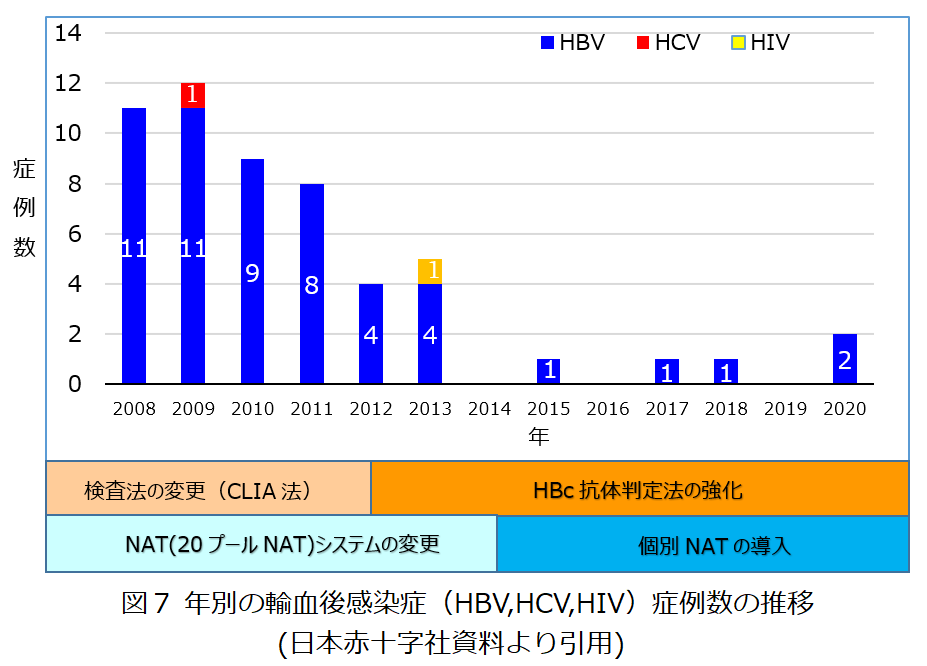
- 輸血医療において,輸血後感染症としてのHBV,HCV,HIVは,克服すべき重要な課題であり,従来より,様々な感染症対策が講じられてきた。血液センターでは,2012年からHBc抗体検査を加え,NAT検査では,当初の500検体プール法(1999年~2000年)から50検体プール法(2000年~2004年) ,20検体プール法(2004年~2014年) ,さらには1検体ずつ個別にNAT(2014年8月~ )が行われるように検査が厳格化されており,図7に示すとおり,輸血後ウイルス感染の報告は激減した。
- しかし,献血者がウイルス感染直後のいわゆる 「感染ごく初期」 の場合,このNATをもってしても検出することは困難であり,検査でウイルスが検出できない時期 (ウインドウピリオド) が発生することになります。 現在は,輸血後のウイルス感染は限りなくゼロに近づいていますが,完全にゼロにすることができないのが現状であります。
- 2004年に改正された 「輸血療法の実施に関する指針」 において,核酸増幅検査,HCVコア抗原検査, HIV抗体検査が輸血後感染症検査 (概ね3ヶ月後) として推奨されるようになり,早期診断・早期治療において一定の役割を果たしてきた。
- 今日,輸血用血液製剤は様々な感染症対策(遡及調査,HBc抗体検査,個別NAT検査の導入)が講じられ大幅に減少したことを受け,2020年3月に改正された指針では,これらの輸血後感染症検査の記載の見直しが行われた。
- これらの状況を踏まえて,HBV,HCV,HIVの輸血後感染症検査に関する対応について日本輸血細胞治療学会としての考え方を以下に示します。
- 輸血は非常に有効な補助療法である反面,一種の臓器移植でもあるため,免疫性副作用,非免疫性副作用の発生は避けられず,また個別NATが導入された現在でも輸血による感染症は100%防止するまでには至っていない。輸血管理部門は,副作用の発生状況を正確に把握するために,副作用に関する報告体制を構築する必要がある。発生した場合には,その原因を調査し,再発を防止するための対策を講じる必要がある。また,その情報を赤十字血液センターや厚生労働省に報告する責務も輸血管理部門にはある。安全で適正な輸血がおこなわれるよう,輸血療法委員会を通じて院内に周知する体制が必要となります。
表1 溶血性貧血の分類 |
||
| 急性溶血性輸血副作用 | 遅発性溶血性輸血副作用 | |
| 発症時間 | 輸血後24時間以内 | 輸血後24時間以上 |
| 溶血部位 | 血管内溶血が大部分 | 血管外溶血が大部分 |
| 概 要 |
ABO不適合輸血が大部分を占める |
輸血前の不規則抗体検査が陰性で,二次免疫応答により増加したIgG同種抗体が原因となる典型的な遅発性溶血性副作用は,輸血後3~14日程度で溶血所見を認める |
急性溶血性輸血副作用(AHTR)
大部分がABO不適合輸血が原因であるが,まれに補体結合性の不規則抗体で認められる。症状としては,輸血開始後5分~15分以内に,静脈に沿った熱感,血管痛,発熱,悪寒戦慄,胸部痛,呼吸困難,腹痛,血圧低下,嘔吐などの症状や所見を認め,ヘモグロビン尿,Hb値の低下,LDHの上昇などの溶血症状を経て,DICによる急性の腎不全によるカリウムの上昇(8mEq/L以上)により,最終的には心室細動により心停止を引き起こす。
①Hbの低下
②LDの上昇
③ヘモグロビン尿
④凝固異常
⑤DAT陽性,クロスマッチ用陽性
⑥クレアチニン上昇
⑦ハプトグロビンの低下
直ちに輸血を中止する必要がある。血管を確保した状態で点滴に代え,全速で滴下する。患者の全身状態をモニターし,呼吸循環状態,尿量保持(>100mL/時)に専念する。利尿剤,ドーパミン,酸素などの保存的治療で対応困難な場合やショック,DIC,腎不全への進展を念頭に治療が後手にならないよう,ICUなどで集中的に対応する。
ABO不適合輸血に関する安全対策は,医療安全対策上,最も重要な対策の一つである。輸血部門が中心となり,院内における輸血実施手順を作成し,事故防止に努めることは重要な業務である。院内での情報発信や定期的な安全対策研修の実施も必要となる。輸血業務に係わる全てのスタッフの知識や意識の向上が,必要と思われる。
遅発性溶血性輸血副作用(DHTR)
輸血あるいは妊娠による抗原刺激で産生した不規則抗体の抗体価は,時間の経過とともに低下する。検出感度以下に低下すると,輸血前検査(不規則抗体検査,クロスマッチ)で検出できなくなる。そのため,不規則抗体の存在に気付かず輸血された赤血球と反応して溶血が起こり,24 時間以降にそれに伴う発熱や貧血,黄疸,Hb 値の低下,LDH・総ビリルビンの上昇,ヘモグロビン尿などの溶血を伴う症状を示す。稀に,腎不全,DICなどによる死亡例もあるが重篤化することは少ない。通常は輸血後,数日から数週間を経てから溶血症状が出現する。
関連する不規則抗体は,Rh系,Kidd系,Duffy系抗体等の量的効果を示す不規則抗体が関与する。
①輸血前の不規則抗体は陰性で,輸血後陽性となる。
②DAT陽性
③溶血所見:Hbの低下,LDやT-Biliの上昇,ヘモグロビン尿
通常は無治療で経過観察するが,腎機能所見には十分な注意が必要である。重度の溶血所見がみられた時はAHTRと同様に治療する。
<免疫学的要因>
発熱
以下の1項目以上の症状を認めた場合を輸血による発熱と定義される。
原因としては,患者が保有する白血球抗体と血液製剤中の白血球抗原との間,もしくは患者の白血球と血液製剤中の白血球抗体の抗原抗体反応によって産生されたサイトカイン(IL-1,IL-6 ,TNF-α)による。
アレルギー反応

輸血関連肺障害(Transfusion Related Acute Lung Injury:TRALI)
| 表2 TRALIの定義 |
| TRALIタイプⅠ |
|
1.急性肺障害(ALI) 2.輸血前にALIを認めない 3.輸血中,輸血後6時間以内に発症 ※ARDSリスクファクターなし |
| TRALIタイプⅡ |
|
※ARDSリスクファクターあり,または経度の既存ARDSあり |
ARDS:急性呼吸窮迫症候群
輸血後紫斑病(Post-transfusion purpura :PTP)
輸血後移植片宿主病(Post-transfusion graft-versus-host disease :PT-GVHD)
<非免疫学的要因>
輸血後関連循環過負荷(Transfusion Associated Circulatory Overload:TACO)
| 表4 TRALIとTACOの特徴 | ||
| 項目 | TRALI | TACO |
| 発熱 |
多い | まれ |
| 血圧 | 低下 | 変化なし,または上昇 |
| 呼吸器症状 | 急性呼吸器不全 | 急性呼吸器不全 |
| 頚動脈 | 不変 | 怒張 |
| 聴診 | ラ音 |
ラ音,心音でS3聴取(+/-) |
| 胸部X線 | 両側肺浸潤頴影 | 両側肺浸潤頴影 |
| 左室駆出率 | 正常または低下 | 低下 |
| 肺動脈楔入圧 | ≦18mmHg | >18mmHg |
| 肺胞惨出液 | 惨出性 | 漏出性 |
| 水分バランス | 正負どちらも有り得る | 正 |
| 利尿剤の効果 | ほとんどなし | 有効 |
| 白血球数 | 一過性の減少 | 不変 |
| BNP | <200pg/mL | >1,200pg/mL |
| 白血球抗体 |
ドナーの白血球抗体陽性でドナー・レシピエント間のクロスマッチ陽性 |
ドナーの白血球抗体の存在は問わないが,陽性に場合はTACOと診断されていてもTRALIの可能性もある |
細菌感染症
血液センターでは,細菌混入を防止するために,表5のようなさまざまな安全対策が講じられている。

| 表5 血液センターにおける細菌混入を防止する安全対策 |
|
□採血時における問診 |
赤血球製剤の有効期限は,採取後21日間であり,通常医療機関に納品される時には1週間くらい経過している場合が多く,場合によっては2週間以上経過した製剤が納品されることもある。図6は赤血球製剤に細菌を接種後の色調の変化をみたものである。通常の赤血球製剤は暗赤色であるのに対し,細菌が混入し長期間保存した赤血球製剤は,細菌が極度に増殖すると著しい溶血を起こす。バック内は溶出したヘモグロビンの色調によって黒色化するため,製剤の異変を肉眼でも確認することができる。セグメント内の赤血球層は通常,正常な色調であるので,バック内の血液との色調比較は,指標の一つとなる。

わが国では,2007年1月から全ての血液製剤において,貯血前白血球除去をおこなっており,血液製剤中の白血球による輸血後の発熱は少なくなった。よって,輸血中,輸血後 表5に示すような症状がみられた場合は,細菌感染症による副作用についても念頭に置き,適正に対応する必要がある。
| 表5 細菌感染症の診断 | |
| 1 |
次の症状のうち,どれか一つ以上が輸血後4時間以内に起こった場合 |
| 2 |
患者血液と原因製剤の確保(同一の菌が検出されれば確定) |
輸血後感染症

- 輸血副作用は,赤血球を主体とした溶血性,それ以外の白血球,血小板,血漿タンパクなどが主な原因となる非溶血性に分類されるが,溶血性をさらに副作用発症までの時間で分類した場合は,発症時間が24時間以内を急性溶血性輸血副作用(AHTR)とし,24時間以降を遅発性溶血性副作用(DHTR)として区別している。
- このセクションでは,主な輸血副作用について紹介する。
- 溶血性輸血副作用は免疫学的な原因により発生し,輸血後24 時間以内の発生か否かにより,急性溶血性輸血副作用と遅発性溶血性輸血副作用に分類される(表1)。
- 非溶血性輸血副作用は,輸血副作用の中で最も多く,副作用の要因から免疫学的要因と非免疫学的要因に分けられる。免疫学的要因には,発熱反応(発熱,悪寒戦慄など),アレルギー反応(蕁麻疹,掻痒感など),輸血関連肺障害(TRALI),輸血後紫斑病(PTP),輸血後移植片宿主病(PT-GVHD)があり,非免疫学的要因には,輸血後関連循環過負荷(TACO),細菌感染症,輸血後感染症がある。
- 免疫反応は,異物(抗原)を排除するために働く生体にとって不可欠な生理機能であるが,時に特定の抗原に対して過剰な反応を示すことがあります。この過剰反応(蕁麻疹,掻痒感,呼吸困難,血圧低下等)をアレルギー反応といい,特に反応が強く,呼吸器・心血管系の症状を伴い血圧低下や意識障害をきたす様な全身性のものをアナフィラキシーと呼ばれています。重篤なアナフィラキシーが起こることはまれであるが,アレルギー反応は輸血副作用のなかではもっとも頻度が高い副作用です。
- 輸血によるアレルギーの原因として特定されているのは,血漿蛋白(IgAやハプトグロビン)欠損患者で過去の輸血等により当該蛋白に対する抗体が産生されている場合のみであり,原因のほとんどは解明されていません。原因物質として特定されてはいませんが,食物アレルギーのある患者に,献血前に当該食物を摂食した献血者の血液を輸血してアレルギーが発生したとの報告があります。
- 対策として,赤血球製剤や血小板製剤の輸血によってアナフィラキシーを繰り返す患者には,洗浄赤血球や洗浄血小板等が有用である。アレルギーの原因が血漿蛋白欠損と特定されている患者に血漿製剤を輸血する際は,当該血漿蛋白欠損の献血者由来の血漿製剤が必要となる場合があるので,血液センターに相談する。抗ヒスタミン剤やステロイドの事前投与には明確なエビデンスはありませんが,予防投与を行う場合には輸血の30~60分前に実施します。
- 輸血後6時間以内に,非心原性の急激な肺水腫による呼吸困難を呈する重篤な副作用である。現在,輸血関連死の主な原因の一つとなっている。
- 発症のメカニズムは,血液製剤中の白血球抗体(HLA抗体,好中球抗体)やその他の未確認物質と患者白血球や肺毛細血管内皮細胞との抗原抗体反応により,好中球が活性化され、肺の毛細血管に損傷を与えることで起こる(図1)。
- 発生頻度であるが,日本赤十字社の報告によると2004年~2011年の間299例の報告があり,17例が死亡している。8万~22万パックに1例の頻度であり,血小板製剤による事例が多い。
- 診断基準については,従来,TRALIとpossible TRALIに分類されていたが,2019年に英国SHOTによりタイプⅠとⅡに再定義された(表2)
- 治療に関しては,まず早期に診断することが重要となってくる。輸血開始後に急激な呼吸障害が現れた場合には,直ちに輸血を中止(ラインは確保)し,呼吸管理を行う必要があります。早期の確定診断には,胸部X線,中心静脈圧,胸部聴診,バイタル,血液ガスなどが有効です。重篤な場合,人工呼吸器の装着などが必要になります。
TRALI発症前後の胸部X線像を示します(図2)。 - TRALIの予防に関しては,妊娠により女性血液中につくられた抗体が原因になっていることが外国での取り組みから明らかであることから,わが国でも2012年から400mL由来のFFPの製造を男性由来のみとしており,FFPによるTRALIの発生は減少してきた。発生原因に関して,白血球抗体や血漿抗体以外の未確認物質による可能性があるため,輸血中・輸血後に十分観察を行い,呼吸器症状がでた場合はTRALIを念頭に置き対処する必要がある。
- 製剤中の血小板抗原(HPA)に対する患者の抗体により,輸血後5日から12日後に発症する血小板減少症で,HLA抗体が原因となる血小板輸血不応と異なり,患者自身の血小板も急激に減少し,出血傾向(粘膜出血,血尿,全身多発性出血斑等)を呈することが特徴である。妊娠や輸血で感作を受けている患者に起こり,主にHPA-1a抗原に対する抗体が関与していると考えられていますが,その他の抗原の関与も示唆されています。患者の血小板が破壊される機序ははっきりしていません。治療としては,IVIGやステロイドの大量投与,血漿交換等が行われます。
- 輸血後GVHDは,輸血用血液製剤中の供血者リンパ球が生着し,患者の体組織を攻撃・傷害することによって起きる病態です(図3)。輸血後1~2週間で発熱・紅斑が出現し,肝障害・下痢・下血等の症状を伴うとともに,骨髄無形成・汎血球減少症,多臓器不全を呈して,ほとんどの症例で輸血から1カ月以内に致死的経過をたどります。
- 輸血後GVHDに関して,有効な治療法はないので,輸血用血液に放射線照射をして予防することが重要となります。わが国では,1998年からFFPを除く全ての血液製剤に放射線照射が実施され対策が取られており,2000年以降,放射線照射血液製剤による輸血後GVHDは報告されていません。
- また,院内採取した同種血の使用に関しては,輸血後GVHD回避のためにも極力避けるべきである。少なくとも,未照射地を輸血してはならない。
- TACOとは,輸血に伴う循環負荷による心不全(図4)であり,呼吸困難,頻脈,血圧上昇などを認める。胸部X線でうっ血性の心不全の所見(図5)を認めることがあり,輸血後6時間以内の発症が多い。
- 症状としては,呼吸困難,起座呼吸,うっ血性心不全,チアノ-ゼ,頻脈,血圧上昇がみられ,補助診断として,BNP,NT-pro BNP,心エコーが有効である。基本的な病態は心不全であり,日本赤十字社における評価基準を表3に示す。確定診断は容易ではなく,虚血性心疾患が存在する場合はTACOとは診断しない。典型的なTRALIとTACOの特徴を表4に示す。
- TACOの発生頻度は,日本赤十字社の報告によると,2016年では33件報告されており,年々増加しています。欧米含め,TACOはABO不適合輸血,TRALIと合わせて,重篤な輸血後関連副作用といわれています。
- TACOはどの年齢層でも発症がみられるが,特に高齢者に多く,赤血球輸血が原因の場合が多い。特に心毒性や慢性貧血などの心機能障害や,腎機能障害をもった患者や,低アルブミン血症,高齢者(特に70歳以上),低体重患者に輸血する場合は,輸血量や速度に注意し,十分観察する必要がある。
- 血液製剤によるウイルス感染については,献血血液へのHBc抗体や個別NATの導入により,感染血液の多くが排除されるようになった。一方で,血液製剤に混入した細菌汚染による輸血後感染症のリスクも存在しており,致死的な合併症となることから,注意する必要がある。日本赤十字社の報告では,1998年~2008年の11年間に366例の輸血後細菌感染疑いが報告されている。
- 輸血医療において,輸血後感染症としてのHBV,HCV,HIVは,克服すべき重要な課題であり,従来より,様々な感染症対策が講じられてきた。血液センターでは,2012年からHBc抗体検査を加え,NAT検査では,当初の500検体プール法(1999年~2000年)から50検体プール法(2000年~2004年) ,20検体プール法(2004年~2014年) ,さらには1検体ずつ個別にNAT(2014年8月~ )が行われるように検査が厳格化されており,図7に示すとおり,輸血後ウイルス感染の報告は激減した。
- しかし,献血者がウイルス感染直後のいわゆる 「感染ごく初期」 の場合,このNATをもってしても検出することは困難であり,検査でウイルスが検出できない時期 (ウインドウピリオド) が発生することになります。 現在は,輸血後のウイルス感染は限りなくゼロに近づいていますが,完全にゼロにすることができないのが現状であります。
- 2004年に改正された 「輸血療法の実施に関する指針」 において,核酸増幅検査,HCVコア抗原検査, HIV抗体検査が輸血後感染症検査 (概ね3ヶ月後) として推奨されるようになり,早期診断・早期治療において一定の役割を果たしてきた。
- 今日,輸血用血液製剤は様々な感染症対策(遡及調査,HBc抗体検査,個別NAT検査の導入)が講じられ大幅に減少したことを受け,2020年3月に改正された指針では,これらの輸血後感染症検査の記載の見直しが行われた。
- これらの状況を踏まえて,HBV,HCV,HIVの輸血後感染症検査に関する対応について日本輸血細胞治療学会としての考え方を以下に示します。
- 輸血は非常に有効な補助療法である反面,一種の臓器移植でもあるため,免疫性副作用,非免疫性副作用の発生は避けられず,また個別NATが導入された現在でも輸血による感染症は100%防止するまでには至っていない。輸血管理部門は,副作用の発生状況を正確に把握するために,副作用に関する報告体制を構築する必要がある。発生した場合には,その原因を調査し,再発を防止するための対策を講じる必要がある。また,その情報を赤十字血液センターや厚生労働省に報告する責務も輸血管理部門にはある。安全で適正な輸血がおこなわれるよう,輸血療法委員会を通じて院内に周知する体制が必要となります。
| 表1 溶血性貧血の分類 | ||
|
急性溶血性輸血副作用 |
遅発性溶血性輸血副作用 |
|
|
発症時間 |
輸血後24時間以内 |
輸血後24時間以上 |
|
溶血部位 |
血管内溶血が大部分 |
血管外溶血が大部分 |
|
概 要 |
ABO不適合輸血が大部分を占める |
輸血前の不規則抗体検査が陰性で,二次免疫応答により増加したIgG同種抗体が原因となる典型的な遅発性溶血性副作用は,輸血後3~14日程度で溶血所見を認める |
急性溶血性輸血副作用(AHTR)
大部分がABO不適合輸血が原因であるが,まれに補体結合性の不規則抗体で認められる。症状としては,輸血開始後5分~15分以内に,静脈に沿った熱感,血管痛,発熱,悪寒戦慄,胸部痛,呼吸困難,腹痛,血圧低下,嘔吐などの症状や所見を認め,ヘモグロビン尿,Hb値の低下,LDHの上昇などの溶血症状を経て,DICによる急性の腎不全によるカリウムの上昇(8mEq/L以上)により,最終的には心室細動により心停止を引き起こす。
 ①Hbの低下
①Hbの低下②LDの上昇
③ヘモグロビン尿
④凝固異常
⑤DAT陽性,クロスマッチ用陽性
⑥クレアチニン上昇
⑦ハプトグロビンの低下
直ちに輸血を中止する必要がある。血管を確保した状態で点滴に代え,全速で滴下する。患者の全身状態をモニターし,呼吸循環状態,尿量保持(>100mL/時)に専念する。利尿剤,ドーパミン,酸素などの保存的治療で対応困難な場合やショック,DIC,腎不全への進展を念頭に治療が後手にならないよう,ICUなどで集中的に対応する。
ポイント
O型のヒトにある抗A,抗B抗体は,A型やB型のヒトが持つ抗B抗体,抗A抗体に比べて,通常抗体価が高いため,患者がO型で輸血量が多ければ多いほど重篤になりやすい。
ABO不適合輸血に関する安全対策は,医療安全対策上,最も重要な対策の一つである。輸血部門が中心となり,院内における輸血実施手順を作成し,事故防止に努めることは重要な業務である。院内での情報発信や定期的な安全対策研修の実施も必要となる。輸血業務に係わる全てのスタッフの知識や意識の向上が,必要と思われる。
遅発性溶血性輸血副作用(DHTR)
輸血あるいは妊娠による抗原刺激で産生した不規則抗体の抗体価は,時間の経過とともに低下する。検出感度以下に低下すると,輸血前検査(不規則抗体検査,クロスマッチ)で検出できなくなる。そのため,不規則抗体の存在に気付かず輸血された赤血球と反応して溶血が起こり,24 時間以降にそれに伴う発熱や貧血,黄疸,Hb 値の低下,LDH・総ビリルビンの上昇,ヘモグロビン尿などの溶血を伴う症状を示す。稀に,腎不全,DICなどによる死亡例もあるが重篤化することは少ない。通常は輸血後,数日から数週間を経てから溶血症状が出現する。
関連する不規則抗体は,Rh系,Kidd系,Duffy系抗体等の量的効果を示す不規則抗体が関与する。
通常は無治療で経過観察するが,腎機能所見には十分な注意が必要である。重度の溶血所見がみられた時はAHTRと同様に治療する。
<免疫学的要因>
発熱
 以下の1項目以上の症状を認めた場合を輸血による発熱と定義される。
以下の1項目以上の症状を認めた場合を輸血による発熱と定義される。
原因としては,患者が保有する白血球抗体と血液製剤中の白血球抗原との間,もしくは患者の白血球と血液製剤中の白血球抗体の抗原抗体反応によって産生されたサイトカイン(IL-1,IL-6 ,TNF-α)による。
アレルギー反応

輸血関連肺障害(TRALI)
-Transfusion Related Acute Lung Injury-

| 表2 TRALIの定義 |
|
TRALIタイプⅠ |
|
1.急性肺障害(ALI) 2.輸血前にALIを認めない 3.輸血中,輸血後6時間以内に発症 ※ARDSリスクファクターなし |
|
TRALIタイプⅡ |
|
※ARDSリスクファクターあり,または経度の既存ARDSあり |
ARDS:急性呼吸窮迫症候群

輸血後紫斑病(PTP)
-Post-transfusion purpura-
輸血後移植片宿主病(PT-GVHD)
-Post-transfusion graft-versus-host disease-

<非免疫学的要因>
輸血後関連循環過負荷(TACO)
-Transfusion Associated Circulatory Overload-


| 表4 TRALIとTACOの特徴 | ||
|
項目 |
TRALI |
TACO |
|
発熱 |
多い |
まれ |
|
血圧 |
低下 |
変化なし,または上昇 |
|
呼吸器症状 |
急性呼吸器不全 |
急性呼吸器不全 |
|
頚動脈 |
不変 |
怒張 |
|
聴診 |
ラ音 |
ラ音,心音でS3聴取(+/-) |
|
胸部X線 |
両側肺浸潤頴影 |
両側肺浸潤頴影 |
|
左室駆出率 |
正常または低下 |
低下 |
|
肺動脈楔入圧 |
≦18mmHg |
>18mmHg |
|
肺胞惨出液 |
惨出性 |
漏出性 |
|
水分バランス |
正負どちらも有り得る |
正 |
|
利尿剤の効果 |
ほとんどなし |
有効 |
|
白血球数 |
一過性の減少 |
不変 |
|
BNP |
<200pg/mL |
>1,200pg/mL |
|
白血球抗体 |
ドナーの白血球抗体陽性でドナー・レシピエント間のクロスマッチ陽性 |
ドナーの白血球抗体の存在は問わないが,陽性に場合はTACOと診断されていてもTRALIの可能性もある |
細菌感染症
 血液センターでは,細菌混入を防止するために,表5のようなさまざまな安全対策が講じられている。
血液センターでは,細菌混入を防止するために,表5のようなさまざまな安全対策が講じられている。表5 血液センターにおける細菌混入を防止する安全対策
|
□採血時における問診 |
赤血球製剤の有効期限は,採取後21日間であり,通常医療機関に納品される時には1週間くらい経過している場合が多く,場合によっては2週間以上経過した製剤が納品されることもある。図6は赤血球製剤に細菌を接種後の色調の変化をみたものである。通常の赤血球製剤は暗赤色であるのに対し,細菌が混入し長期間保存した赤血球製剤は,細菌が極度に増殖すると著しい溶血を起こす。バック内は溶出したヘモグロビンの色調によって黒色化するため,製剤の異変を肉眼でも確認することができる。セグメント内の赤血球層は通常,正常な色調であるので,バック内の血液との色調比較は,指標の一つとなる。

わが国では,2007年1月から全ての血液製剤において,貯血前白血球除去をおこなっており,血液製剤中の白血球による輸血後の発熱は少なくなった。よって,輸血中,輸血後 表5に示すような症状がみられた場合は,細菌感染症による副作用についても念頭に置き,適正に対応する必要がある。
|
表5 細菌感染症の診断 |
|
|
1 |
次の症状のうち,どれか一つ以上が |
|
2 |
患者血液と原因製剤の確保(同一の菌が検出されれば確定) |
輸血後感染症


- ページの選択 -




















