➄直接抗グロブリン試験陽性時の対応
- 直接抗グロブリン試験(direct antiglobulin test (DAT) )は,生体内で赤血球に免疫グロブリンや補体が感作しているか否かを検査するために用いられる。よって,DATは自己免疫性溶血性貧血(AIHA),胎児・新生児溶血性疾患(HDFN),不規則抗体に起因する遅発性溶血性副作用(DHTR)の診断に有用である。
- 検体は,試験管内補体活性化を阻止するため,抗凝固剤(EDTAや クエン酸塩)で採血した血液が望ましい。冷蔵庫で保存した血液は,寒冷凝集素とともに補体が感作することがあり,生体内の反応か生体外の反応か区別できないため,原則的には使用しない。
- IgG,補体いずれにも反応する多特異抗ヒトグロブリン試薬を用いる。特異性を確認するには,抗IgG試薬,抗C3d試薬などの単特異性の試薬を用いる。
- まず,多特異抗ヒトグロブリン試薬を用いて判定する(表1)。対照が陽性になった場合は,寒冷凝集素あるいは冷式抗体が反応している可能性があるので,37℃加温後判定する。また,血球を十分に洗浄することで連銭形成の影響を回避することができる。DAT陽性の原因の追究が必要な場合は,単特異性試薬を用いることで典型的な病態を推測することができる(表2)。
- DAT陽性患者でさらに精査が必要かどうか,また血液製剤の選択が必要かどうかについては,溶血所見の有無,AIHA患者かどうか,血漿中に同種抗体が存在するかどうかで異なってくる。まず,AIHAと診断がつけば,副腎皮質ステロイド薬による治療が第一選択となり,輸血をしなくて良いケースがでてくる。
- 次に,自己対照・DATに影響を与える,患者の疾患名(自己免疫疾患,SLE,AIHAなど),投与薬剤,輸血歴(過去3ヶ月以内)を確認することが重要となります。経験上,抗生物質(セフェム系,ペニシリン系の抗生物質など)を投与されている患者は自己対照陽性になります。取り扱い説明書を見ると,臨床検査に及ぼす影響の項目で 「直接クームス試験が陽性なることがあります。」 と記載されている薬剤があります。
- 患者赤血球上及び血漿中に自己抗体と同種抗体が共存している場合がある。その場合,自己抗体を吸着後同種抗体の有無を確認することが重要になってきます。
- DATが陽性であっても,不規則抗体スクリーニングが陰性の場合は血液製剤の選択に支障をきたすことは無いので,それ以上の精査は必要ない。ただし,患者が3ヶ月以内に輸血を受けており,DHTRが疑われる場合やHDFNが疑われる新生児では精査が必要となる。同種抗体が輸血された赤血球や患児赤血球に全て結合している場合が稀に考えられるからであり,その場合は,患者赤血球から結合した同種抗体を解離し,解離液中の特異性を調べる必要がある。
- DIIHAは免疫機序の観点から,薬剤吸着型,免疫複合体型,赤血球自己抗体型,膜修飾型の4種類があり,薬剤,薬剤と赤血球抗原の複合体,赤血球抗原のいずれかに対する抗体が産生され,その抗体により血管外溶血が引き起こされることがある。
- それぞれの免疫機序と関連のある薬剤を下記に示します。
- 2016年度の一年間に全国で供給された赤血球製剤は3,284,104 本であり,このうちDAT陽性の苦情は,全国で499 本(0.015%)あり,赤血球製剤の6,581本に1本の割合であったと報告されている。これらの原因を調べた調査では,全体の72%がw+〜1+の弱陽性であり,その56%の原因が赤血球抗体では無く,セグメント内の血漿中に存在するγ-グロブリンなどによる非特異反応であったとしている。
- DAT陽性の血液を輸血した場合のリスクについては,ほとんどが弱陽性であり輸血した血液が直ぐに壊される(貪食される)可能性は極めて低く,通常の製剤と同等の輸血効果が得られると考えられるが,溶血を否定するエビデンスがないこと,加えて交差適合試験が陽性になることから,血液センターに返品することが適切だと考えます。
- 輸血検査で異常が観察された場合,自己対照とDATを組み合わせることで,不規則抗体の検出を含めた原因を推定するのに役立ちます(表8)。
- 自己対照の実施に関して, 「赤血球型検査(赤血球系検査)ガイドライン(改訂2版)」 の 5.5 の項で不規則抗体スクリーニング時に,自己対照あるいはDAT試験を含める必要はないと書かれている。さらに,不規則抗体スクリーニングや交差適合試験で平行して行われる自己対照やDAT試験の陽性頻度は,各種論文から見ても2~4%であり,96%以上が陰性となる。さらに,解離試験をおこなっても無反応のものが67%以上見られ,労力の割には,自己抗体や薬剤抗体,輸血による抗体などは少ないことが報告されている。よって,DAT陽性時には,費用対効果を十分考慮し実施することが良いと考える。
- 最近の自己対照,DAT実施に関する知見では,多くの施設がル-チン検査でのACやDATを廃止する傾向があります。これは全自動輸血検査機器の導入におけるコストを考慮していることも一因と思われます。
- まず,自己対照が陽性になった時の手順であるが,非特異反応を除外する目的でDATを実施し,陽性の場合精査を進めるかどうか判断する。溶血性貧血の有無,輸血が必要かどうか調べ,必要が無ければこれ以上の精査は必要ない。SCやCMで陽性となりDAT陽性であれば,AIHAを念頭に置き,自己抗体を吸着し同種抗体の存在を調べる必要がある。同定できれば,対応する抗原陰性の適合血を準備することができる。時間的余裕が無く輸血を優先する場合は,自己抗体で最も多いRh系(41.3%)の不適合を避けるために,患者と同型のRh型を選択
- 同様に薬剤投与に起因するDAT陽性の場合でも,赤血球上に型特異性がみられることは比較的少なく,多くは精査をおこなっても,赤血球試薬との陽性反応はみられない。
- さらに,薬剤が起因となっているDAT陽性では,その精査において陰性判定となることも多く,実際には,生体内での溶血を伴う副作用症状はみられないこともあります。
- 夜間や緊急時の輸血におけるDAT陽性の対応については,時間的余裕がある場合には,精査を行い,適合血,あるいは反応の弱いものを選択することが安全な輸血には重要です。しかし,精査を行う時間的余裕がない場合は,赤血球輸血を行う意義(患者の組織に酸素を供給)と実施しない場合のリスクをどう捉えるかが重要になってきます。 輸血実施の判断は医師の専権事項ですが,試験管内の反応で凝集の有無を確認し,輸血用血液の選択に何が ”better“ か ”best“ かをコンサルトするのは臨床検査技師に与えられた使命と考えます。そのため,DAT陽性の精査は主治医との連携を計りながら,進めることが必要になります。
| 表1 DATの反応と判定結果 | |||
| DAT (多特異抗ヒトグロブリン) |
対照(生食) | 判定 | |
| 反応結果 | 0 | 0 | 陰性 |
| + | 0 | 陽性 | |
| + | + | 判定保留 ※1 | |
| 表2 単特異性の反応と考慮すべき病態 | ||||
| 抗IgG | 抗補体 | 対象(生食) | 典型的な病態 | |
| 反応結果 |
+ | 0 | 0 | 自己免疫性溶血性貧血 遅発性溶血性輸血副作用(DHTR) 胎児・新生児溶血性疾患(HDFN) 薬剤起因性溶血性貧血(ぺニシリン型)など |
| + | + | 0 | 自己免疫性溶血性貧血など |
|
| 0 | + | 0~+ | 発作性夜間血色素尿症 発作性寒冷血色素尿症(PCH) 薬剤起因性溶血性貧血 (免疫複合体,寒冷凝集素症(CAS)など) |
|
DAT陽性(抗IgG+)になった場合,可能であればDT解離試験を実施して解離液中に赤血球と特異的に反応する抗体が無いか確認する。3ヶ月以内に輸血歴がある場合は,最近受けた輸血により不規則抗体を産生しはじめ,輸血した血球と反応している可能性がありますので要注意です。
3ヶ月以内に輸血歴が無い患者では,患者赤血球を用いて自己抗体を吸着することができる。ただし,既に多量の自己抗体が結合した患者赤血球をそのまま使用しても,血漿中の自己抗体を効率よく吸着することはできないので,患者赤血球に結合した自己抗体を前もって解離する必要がある。自己抗体の解離法には,PEG吸着法,ZZAP吸着法がある。
3ヶ月以内に輸血歴がある場合は,輸血された赤血球が共存しており,血漿中の同種抗体が吸着してしまうため用いることはできません。
自己抗体吸着後の血漿を用いて不規則抗体スクリーニングを実施する。陰性の場合は,自己抗体のみと考えられるので,通常血液製剤の選択の必要はない。陽性の場合は,同種抗体の特異性を確認し,抗体が同定されれば,抗原陰性の適合血を選択する。
DAT陽性患者の血液型判定には注意が必要である。Duffy血液型や Diego血液型など抗原の有無をIATで確認する場合は,患者赤血球から自己抗体を解離した赤血球を用いて血液型を確認する必要がある。Rh血液型やKidd血液型などモノクローナル抗体試薬を用いて判定する場合は,自己抗体の影響は受けない。その場合,陰性対照が必要となる。
AIHA患者の40~50%に同種抗体を保有しているという報告もあり,抗体を保有している場合対応する抗原陰性の適合血を選択する必要がある。
患者赤血球から自己抗体を解離し,特異性がみられる場合もあるが,多くの自己抗体は全ての赤血球と反応する事が多い。輸血の緊急度によって対応が異なるが,余裕があるなら同種抗体を産生するリスクを低くするため,臨床的意義の高いRh血液型が同型の血液製剤を選択する必要がある。
| 表3 自己免疫性溶血性貧血患者の適合血の選択 | |||
| 溶血症状 | 結合抗体の特異性 | 同種抗体の有無 | 抗原陰性血の選択 |
| なし |
考慮しなくて良い |
(-) | 必要なし |
| (+) 例:抗 |
同種抗体の対応抗原陰性血 例:E(-) |
||
| あり |
なし | (-) | 必要なし |
| (+) 例:抗E |
同種抗体の対応抗原陰性血 例:E(-) |
||
| あり 例:抗Jka |
(-) | 自己抗体の対応抗原陰性血 | |
| (+) 例:抗Jka |
同種抗体の対応抗原陰性血 例:抗Jka |
||
37℃以下で反応する自己抗体によって生じる。自己抗体はほとんどが抗Iであることが多く,成人赤血球を凝集させるが,臍帯血はi型のため反応しない。検査の進め方としては,AIHA患者同様に自己抗体を吸収した血漿(血清)を用いて同種抗体を確認する。寒冷自己抗体を吸収するときは,4℃で実施する。貧血に関しては,多くの症例で寒冷な環境やその他の溶血の誘因を避けることで改善する。
PCH患者の自己抗体(ドナート・ランドシュタイナー抗体)は,四肢などの体の低温部で赤血球を反応後,不可逆的にC3,C4を古典的経路を介して活性化し溶血させるが,37℃では自己抗体は赤血球から解離する。自己抗体が4℃以上で反応することはなく,輸血検査で問題になることはない。
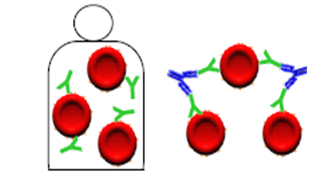
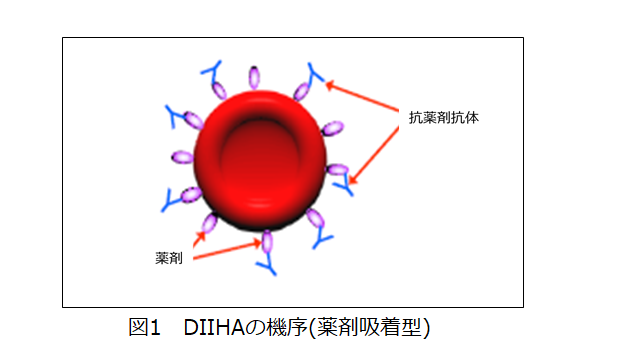
抗薬剤抗体が,赤血球上に硬く結合した大量の薬剤と反応することによりDATが陽性になる。抗IgG試薬を用いたDATで陽性となる。通常,補体は活性化されず,溶血は血管外溶血の機序による(図1,表4)。
| 表4 薬剤吸着型と関連のある薬剤 |
||
| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
| ペニシリン(アモキシシリン) | サワシリン,パセトシン | 抗菌薬 |
| シスプラスチン | ランダ,ブリプラチン | 抗悪性腫瘍薬 |
| エルスロマイシン | エリスロット | 抗菌薬 |
| トルブタマイド | ジアベン,ラスチノン | 糖尿病治療薬 |
| セファロチン | ケブリン | 抗菌薬 |
| セファゾリン | セファメジン | 抗菌薬 |
| テトラサイクリン | アクロマイシン | 抗菌薬 |
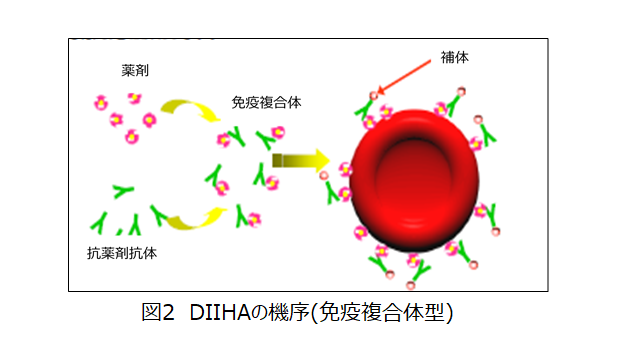
抗薬剤抗体が,薬剤に対する特異抗体として免疫複合体を形成する。この複合体が非特異的に赤血球表面に結合し,補体を活性化することにより血管内溶血を誘発する。血清(血漿)は薬剤存在下でのみ赤血球と反応し解離液は反応しない。DIIHAの原因としては最も低頻度である。通常補体試薬によってDAT陽性となるが,時にIgGによることもある。適合血の選択は必要ありません。(図2,表5)
| 表5 免疫複合体型と関連のある薬剤 | ||
| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
| アセトアミノフェン | カロナール | 非ステロイド抗炎症薬 |
| キニン | 塩酸キニーネ,硫酸キニーネ | 抗マラリア薬 |
| キニジン | 硫酸キニジン | 抗不整脈薬 |
| リファンピシン | リファジン | 抗結核薬 |
| ストレプトマイシン | 硫酸ストレプトマイシン | 抗結核薬 |
| セフォテダン |
ヤマテタン,セフォテタン |
抗菌薬 |
| セファタキシム | グラフォラン,セフォタックス | 抗菌薬 |
| セフチドキシム | エポセリン | 抗菌薬 |
| クロルプロマジン | ウンタミン,コントミン | 抗精神薬 |
| フルオロウラシル | 5-FU | 抗悪性腫瘍薬 |
| メソトレキサート(MTX) |
メソトレキセート | 抗悪性腫瘍薬,抗リウマチ薬 |
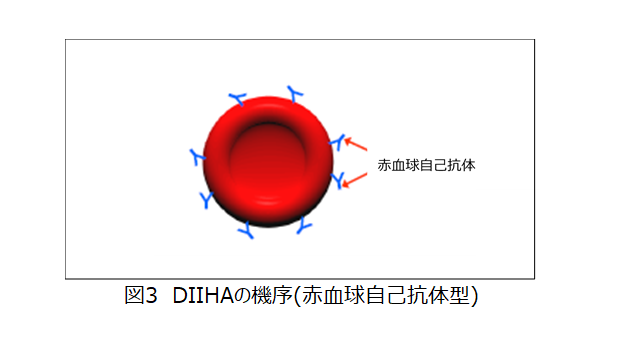
α-メチルドーパに代表される薬剤では,AIHAと症状,検査所見などがまったく同じ様なIgG型赤血球自己抗体が産生されることがあり,突発性AIHAとの鑑別が困難な場合があります。自己抗体産生メカニズムは不明です。(図3,表6)
| 表6 赤血球自己抗体型と関連のある薬剤 | ||
| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
| α-メチルドーパ | アルドメッド | 高圧剤 |
| レボドーパ | ドバゾール、ドバストン,ドバール | パーキンソン病治療薬 |
| メフェナム酸 | ポンタール | 抗炎症解熱鎮痛薬 |
| プロカインアミド | アミサリン | 抗不整脈薬 |
| イブプロフェン | ブルフェン,パブロンエース,ベンザブロック,ストナ | 非ステロイド抗炎症剤 |
| スリンダク | クリノリル | 抗炎症薬 |
| ジフェニルヒダントイン | フェントイン | 抗てんかん薬 |
| フルダラビン | フルダラ | 抗悪性腫瘍薬 |
| フェノブロフェン | フェノブロン | 非ステロイド抗炎症剤 |
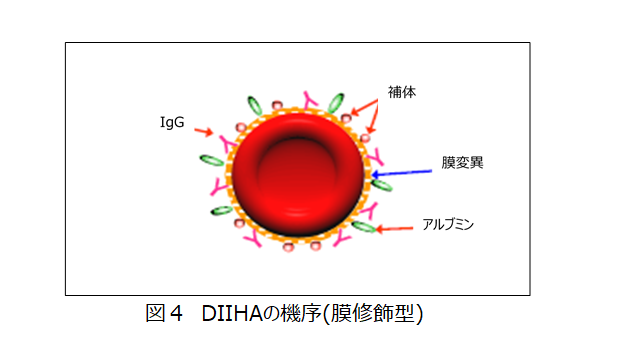
ある種の薬剤は,赤血球膜を変異(修飾)し,非特異的にアルブミン,グロブリン,補体などの全ての蛋白を吸着させると考えられています。通常抗体解離液は反応しません。溶血性貧血の原因となることが稀にある。適合血の選択は必要ありません。(図4,表7)
| 表7 修飾型と関連のある薬剤 | ||
| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
| セファロスポリン(第一世代) セファゾリン セファロチン セファレキシン セファドロキシル |
セファメジン ケフリン ケフレックス セファドリル |
抗菌薬 |
| シスプラスチン | ランダ、ブリプラチン | 抗悪性腫瘍薬 |
| スルバクタムナトリウム | ユナシン | 抗菌薬 |
| スラミン | ゲルマニン | 抗トリパノソーマ剤,抗フィラリア剤 |
| 表8 輸血検査・異常反応の推定 | |||
| 患者血清+ 検査赤血球 (SC or CM) |
患者血清+ 患者赤血球 (AC) |
患者赤血球 (DAT) |
解 釈 |
| + | - | - | 不規則抗体陽性 |
| + | + | + | 血清,血球に自己抗体の存在 不適合輸血 |
| - | + | + | 血球に自己抗体の結合 血球に薬剤起因性抗体の結合 血球膜の変性による蛋白の結合 |
| + | + | - | 試薬による非特異反応 高蛋白による連銭形成 補液成分の混入による連銭形成 |
SC:抗体スクリ-ニング CM:交差適合試験 AC:自己対照 DAT:直接抗グロブリン試験
- 直接抗グロブリン試験(direct antiglobulin test (DAT) )は,生体内で赤血球に免疫グロブリンや補体が感作しているか否かを検査するために用いられる。よって,DATは自己免疫性溶血性貧血(AIHA),胎児・新生児溶血性疾患(HDFN),不規則抗体に起因する遅発性溶血性副作用(DHTR)の診断に有用である。
- 検体は,試験管内補体活性化を阻止するため,抗凝固剤(EDTAや クエン酸塩)で採血した血液が望ましい。冷蔵庫で保存した血液は,寒冷凝集素とともに補体が感作することがあり,生体内の反応か生体外の反応か区別できないため,原則的には使用しない。
- IgG,補体いずれにも反応する多特異抗ヒトグロブリン試薬を用いる。特異性を確認するには,抗IgG試薬,抗C3d試薬などの単特異性の試薬を用いる。
- まず,多特異抗ヒトグロブリン試薬を用いて判定する(表1)。対照が陽性になった場合は,寒冷凝集素あるいは冷式抗体が反応している可能性があるので,37℃加温後判定する。また,血球を十分に洗浄することで連銭形成の影響を回避することができる。DAT陽性の原因の追究が必要な場合は,単特異性試薬を用いることで典型的な病態を推測することができる(表2)。
- DAT陽性患者でさらに精査が必要かどうか,また血液製剤の選択が必要かどうかについては,溶血所見の有無,AIHA患者かどうか,血漿中に同種抗体が存在するかどうかで異なってくる。まず,AIHAと診断がつけば,副腎皮質ステロイド薬による治療が第一選択となり,輸血をしなくて良いケースがでてくる。
- 次に,自己対照・DATに影響を与える,患者の疾患名(自己免疫疾患,SLE,AIHAなど),投与薬剤,輸血歴(過去3ヶ月以内)を確認することが重要となります。経験上,抗生物質(セフェム系,ペニシリン系の抗生物質など)を投与されている患者は自己対照陽性になります。取り扱い説明書を見ると,臨床検査に及ぼす影響の項目で 「直接クームス試験が陽性なることがあります。」 と記載されている薬剤があります。
- 患者赤血球上及び血漿中に自己抗体と同種抗体が共存している場合がある。その場合,自己抗体を吸着後同種抗体の有無を確認することが重要になってきます。
- DATが陽性であっても,不規則抗体スクリーニングが陰性の場合は血液製剤の選択に支障をきたすことは無いので,それ以上の精査は必要ない。ただし,患者が3ヶ月以内に輸血を受けており,DHTRが疑われる場合やHDFNが疑われる新生児では精査が必要となる。同種抗体が輸血された赤血球や患児赤血球に全て結合している場合が稀に考えられるからであり,その場合は,患者赤血球から結合した同種抗体を解離し,解離液中の特異性を調べる必要がある。
- DIIHAは免疫機序の観点から,薬剤吸着型,免疫複合体型,赤血球自己抗体型,膜修飾型の4種類があり,薬剤,薬剤と赤血球抗原の複合体,赤血球抗原のいずれかに対する抗体が産生され,その抗体により血管外溶血が引き起こされることがある。
- それぞれの免疫機序と関連のある薬剤を下記に示します。
- 2016年度の一年間に全国で供給された赤血球製剤は3,284,104 本であり,このうちDAT陽性の苦情は,全国で499 本(0.015%)あり,赤血球製剤の6,581本に1本の割合であったと報告されている。これらの原因を調べた調査では,全体の72%がw+〜1+の弱陽性であり,その56%の原因が赤血球抗体では無く,セグメント内の血漿中に存在するγ-グロブリンなどによる非特異反応であったとしている。
- DAT陽性の血液を輸血した場合のリスクについては,ほとんどが弱陽性であり輸血した血液が直ぐに壊される(貪食される)可能性は極めて低く,通常の製剤と同等の輸血効果が得られると考えられるが,溶血を否定するエビデンスがないこと,加えて交差適合試験が陽性になることから,血液センターに返品することが適切だと考えます。
- 輸血検査で異常が観察された場合,自己対照とDATを組み合わせることで,不規則抗体の検出を含めた原因を推定するのに役立ちます(表8)。
- 自己対照の実施に関して, 「赤血球型検査(赤血球系検査)ガイドライン(改訂2版)」 の 5.5 の項で不規則抗体スクリーニング時に,自己対照あるいはDAT試験を含める必要はないと書かれている。さらに,不規則抗体スクリーニングや交差適合試験で平行して行われる自己対照やDAT試験の陽性頻度は,各種論文から見ても2~4%であり,96%以上が陰性となる。さらに,解離試験をおこなっても無反応のものが67%以上見られ,労力の割には,自己抗体や薬剤抗体,輸血による抗体などは少ないことが報告されている。よって,DAT陽性時には,費用対効果を十分考慮し実施することが良いと考える。
- 最近の自己対照,DAT実施に関する知見では,多くの施設がル-チン検査でのACやDATを廃止する傾向があります。これは全自動輸血検査機器の導入におけるコストを考慮していることも一因と思われます。
- まず,自己対照が陽性になった時の手順であるが,非特異反応を除外する目的でDATを実施し,陽性の場合精査を進めるかどうか判断する。溶血性貧血の有無,輸血が必要かどうか調べ,必要が無ければこれ以上の精査は必要ない。SCやCMで陽性となりDAT陽性であれば,AIHAを念頭に置き,自己抗体を吸着し同種抗体の存在を調べる必要がある。同定できれば,対応する抗原陰性の適合血を準備することができる。時間的余裕が無く輸血を優先する場合は,自己抗体で最も多いRh系(41.3%)の不適合を避けるために,患者と同型のRh型を選択
- 同様に薬剤投与に起因するDAT陽性の場合でも,赤血球上に型特異性がみられることは比較的少なく,多くは精査をおこなっても,赤血球試薬との陽性反応はみられない。
- さらに,薬剤が起因となっているDAT陽性では,その精査において陰性判定となることも多く,実際には,生体内での溶血を伴う副作用症状はみられないこともあります。
- 夜間や緊急時の輸血におけるDAT陽性の対応については,時間的余裕がある場合には,精査を行い,適合血,あるいは反応の弱いものを選択することが安全な輸血には重要です。しかし,精査を行う時間的余裕がない場合は,赤血球輸血を行う意義(患者の組織に酸素を供給)と実施しない場合のリスクをどう捉えるかが重要になってきます。 輸血実施の判断は医師の専権事項ですが,試験管内の反応で凝集の有無を確認し,輸血用血液の選択に何が ”better“ か ”best“ かをコンサルトするのは臨床検査技師に与えられた使命と考えます。そのため,DAT陽性の精査は主治医との連携を計りながら,進めることが必要になります。

|
表1 DATの反応と判定結果 |
|||
|
|
DAT (多特異抗ヒトグロブリン) |
対照(生食) |
判定 |
|
反応結果 |
0 | 0 |
陰性 |
| + | 0 |
陽性 |
|
| + | + |
判定保留※1 |
|
※1:寒冷凝集素,冷式抗体あるいは強い連銭形成の可能性
|
表2 単特異性の反応と考慮すべき病態 |
||||
|
抗IgG |
抗補体 |
対象 |
典型的な病態 |
|
|
反応 |
+ |
0 |
0 |
自己免疫性溶血性貧血 |
|
+ |
+ |
0 |
自己免疫性溶血性貧血など |
|
|
0 |
+ |
0~+ |
発作性夜間血色素尿症 |
|
DAT陽性(抗IgG+)になった場合,可能であればDT解離試験を実施して解離液中に赤血球と特異的に反応する抗体が無いか確認する。3ヶ月以内に輸血歴がある場合は,最近受けた輸血により不規則抗体を産生しはじめ,輸血した血球と反応している可能性がありますので要注意です。
3ヶ月以内に輸血歴が無い患者では,患者赤血球を用いて自己抗体を吸着することができる。ただし,既に多量の自己抗体が結合した患者赤血球をそのまま使用しても,血漿中の自己抗体を効率よく吸着することはできないので,患者赤血球に結合した自己抗体を前もって解離する必要がある。自己抗体の解離法には,PEG吸着法,ZZAP吸着法がある。
3ヶ月以内に輸血歴がある場合は,輸血された赤血球が共存しており,血漿中の同種抗体が吸着してしまうため用いることはできません。
自己抗体吸着後の血漿を用いて不規則抗体スクリーニングを実施する。陰性の場合は,自己抗体のみと考えられるので,通常血液製剤の選択の必要はない。陽性の場合は,同種抗体の特異性を確認し,抗体が同定されれば,抗原陰性の適合血を選択する。
DAT陽性患者の血液型判定には注意が必要である。Duffy血液型や Diego血液型など抗原の有無をIATで確認する場合は,患者赤血球から自己抗体を解離した赤血球を用いて血液型を確認する必要がある。Rh血液型やKidd血液型などモノクローナル抗体試薬を用いて判定する場合は,自己抗体の影響は受けない。その場合,陰性対照が必要となる。
AIHA患者の40~50%に同種抗体を保有しているという報告もあり,抗体を保有している場合対応する抗原陰性の適合血を選択する必要がある。
患者赤血球から自己抗体を解離し,特異性がみられる場合もあるが,多くの自己抗体は全ての赤血球と反応する事が多い。輸血の緊急度によって対応が異なるが,余裕があるなら同種抗体を産生するリスクを低くするため,臨床的意義の高いRh血液型が同型の血液製剤を選択する必要がある。
|
表3 自己免疫性溶血性貧血患者の適合血の選択 |
|||
|
溶血症状 |
結合抗体 |
同種抗体 |
抗原陰性血 |
|
なし |
考慮しなくて良い |
(-) |
必要なし |
|
(+) |
同種抗体の |
||
|
あり |
なし |
(-) |
必要なし |
|
(+) |
同種抗体の |
||
|
あり |
(-) |
自己抗体の |
|
|
(+) |
同種抗体の |
||
37℃以下で反応する自己抗体によって生じる。自己抗体はほとんどが抗Iであることが多く,成人赤血球を凝集させるが,臍帯血はi型のため反応しない。検査の進め方としては,AIHA患者同様に自己抗体を吸収した血漿(血清)を用いて同種抗体を確認する。寒冷自己抗体を吸収するときは,4℃で実施する。貧血に関しては,多くの症例で寒冷な環境やその他の溶血の誘因を避けることで改善する。
PCH患者の自己抗体(ドナート・ランドシュタイナー抗体)は,四肢などの体の低温部で赤血球を反応後,不可逆的にC3,C4を古典的経路を介して活性化し溶血させるが,37℃では自己抗体は赤血球から解離する。自己抗体が4℃以上で反応することはなく,輸血検査で問題になることはない。
抗薬剤抗体が,赤血球上に硬く結合した大量の薬剤と反応することによりDATが陽性になる。抗IgG試薬を用いたDATで陽性となる。通常,補体は活性化されず,溶血は血管外溶血の機序による(図1,表4)。

| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
| ペニシリン(アモキシシリン) | サワシリン,パセトシン | 抗菌薬 |
| シスプラスチン | ランダ,ブリプラチン | 抗悪性腫瘍薬 |
| エルスロマイシン | エリスロット | 抗菌薬 |
| トルブタマイド | ジアベン,ラスチノン | 糖尿病治療薬 |
| セファロチン | ケブリン | 抗菌薬 |
| セファゾリン | セファメジン | 抗菌薬 |
| テトラサイクリン | アクロマイシン | 抗菌薬 |
抗薬剤抗体が,薬剤に対する特異抗体として免疫複合体を形成する。この複合体が非特異的に赤血球表面に結合し,補体を活性化することにより血管内溶血を誘発する。血清(血漿)は薬剤存在下でのみ赤血球と反応し解離液は反応しない。DIIHAの原因としては最も低頻度である。通常補体試薬によってDAT陽性となるが,時にIgGによることもある。適合血の選択は必要ありません。(図2,表5)

| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
|
アセトアミノフェン |
カロナール |
非ステロイド抗炎症薬 |
|
キニン |
塩酸キニーネ,硫酸キニーネ |
抗マラリア薬 |
|
キニジン |
硫酸キニジン |
抗不整脈薬 |
|
リファンピシン |
リファジン |
抗結核薬 |
|
ストレプトマイシン |
硫酸ストレプトマイシン |
抗結核薬 |
|
セフォテダン |
ヤマテタン,セフォテタン |
抗菌薬 |
|
セファタキシム |
グラフォラン,セフォタックス |
抗菌薬 |
|
セフチドキシム |
エポセリン |
抗菌薬 |
|
クロルプロマジン |
ウンタミン,コントミン |
抗精神薬 |
|
フルオロウラシル |
5-FU |
抗悪性腫瘍薬 |
|
メソトレキサート(MTX) |
メソトレキセート |
抗悪性腫瘍薬, |
|
表5 免疫複合体型と関連のある薬剤 |
||
α-メチルドーパに代表される薬剤では,AIHAと症状,検査所見などがまったく同じ様なIgG型赤血球自己抗体が産生されることがあり,突発性AIHAとの鑑別が困難な場合があります。自己抗体産生メカニズムは不明です。(図3,表6)

| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
|
α-メチルドーパ |
アルドメッド |
高圧剤 |
|
レボドーパ |
ドバゾール,ドバストン,ドバール |
パーキンソン病治療薬 |
|
メフェナム酸 |
ポンタール |
抗炎症解熱鎮痛薬 |
|
プロカインアミド |
アミサリン |
抗不整脈薬 |
|
イブプロフェン |
ブルフェン,パブロンエース,ベンザブロック,ストナ |
非ステロイド抗炎症剤 |
|
スリンダク |
クリノリル |
抗炎症剤 |
|
ジフェニルヒダントイン |
フェントイン |
抗てんかん薬 |
|
フルダラビン |
フルダラ |
抗悪性腫瘍薬 |
|
フェノブロフェン |
フェノブロン |
非ステロイド抗炎症剤 |
|
表6 赤血球自己抗体型と関連のある薬剤 |
||
ある種の薬剤は,赤血球膜を変異(修飾)し,非特異的にアルブミン,グロブリン,補体などの全ての蛋白を吸着させると考えられています。通常抗体解離液は反応しません。溶血性貧血の原因となることが稀にある。適合血の選択は必要ありません。(図4,表7)

| 薬剤名(一般名) | 薬剤名(販売名) | 分類 |
|
セファロスポリン |
|
抗菌薬 |
|
シスプラスチン |
ランダ,ブリプラチン |
抗悪性腫瘍薬 |
|
スルバクタムナトリウム |
ユナシン |
抗菌薬 |
|
スラミン |
ゲルマニン |
抗トリパノソーマ剤, |
|
表7 修飾型と関連のある薬剤 |
||
| 表8 輸血検査・異常反応の推定 | |||
|
患者血清+ |
患者血清+ |
患者赤血球 |
解 釈 |
|
+ |
- |
- |
不規則抗体陽性 |
|
+ |
+ |
+ |
血清,血球に自己抗体の存在 |
|
- |
+ |
+ |
血球に自己抗体の結合 |
|
+ |
+ |
- |
試薬による非特異反応 |
SC:抗体スクリ-ニング CM:交差適合試験 AC:自己対照
DAT:直接抗グロブリン試験




















