新型コロナ検査受託について
- 謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを
賜り厚くお礼申し上げます。 - 2022年度版検査案内に記載の通り、令和4年度診療報酬改定にて下記項目の診療報酬
が700点へ変更予定でしたが、令和4年3月16日付け厚生労働省保険局医療課長の通知
「保医発0316第1号」により一部変更が通知されましたのでご案内いたします。 - ご利用の先生方には大変ご迷惑をおかけすることと存じますが、何卒ご了承賜ります
ようよろしくお願い申し上げます。 - 謹白
- 記
- 【適用日】 2022年 4月 1日 (金)から適用
- 2021年6月29日(火)ご依頼分より変異株解析検査対象に追加
- 2021年6月21日(月)受付分より
- 謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを
賜り厚くお礼申し上げます。 - この度、下記の検査項目につきまして、新たに受託開始、及び受託中止をさせて
いただくこととなりましたので謹んでご案内申し上げます。 - 先生方には何卒ご利用いただきますよう、よろしくお願い申し上げます。
- 謹白
- 記
- 2021年 6月18日(金)ご依頼分より開始
- [実施日] 2021年 5月 8日(土)ご依頼分より
- [変異株スクリーニング検査追加対象項目]
- 2021年1月10日・11日の連休における新型コロナウイルスPCR検査体制についてお知らせします。
- 検査項目【0987】新型コロナウイルス RNA 定性は、2021 年 1 月 11 日(月)の15:00までに所定場所(本社コロナ検査検体搬入場所)に搬入された検体について、1月10日(日)搬入分と合わせて、1月11日に検査を行います(1 月 10 日は検査を行いません)。
- 至急FAX 分については1月11日(月)検査終了後に報告します。報告書は1月13日(水)の報告となります。
- 2020年12月28日から2021年1月5日における新型コロナウイルスPCR検査体制についてお知らせします。
- ドイツの空港における新型コロナウイルス検査への高感度抗原検査試薬・検査機器の供給について
- 弊社グループ会社である富士レビオ・ホールディングス株式会社傘下の Fujirebio Europe N.V.(CEO:Christiaan De Wilde、ベルギー)は、欧州で遺伝子関連検査ビジネスを手掛けるCENTOGENE GmbH(CEO:Dr. Arndt Rolfs、ドイツ、以下「Centogene 社」)との間で、全自動化学発光酵素免疫測定システム「ルミパルス® G1200」および高感度抗原検査試薬「ルミパルス SARS-CoV-2Ag」を供給することで合意いたしました。
- Centogene 社は、ドイツの主要空港において新型コロナウイルスの PCR 検査を旅行者および空港勤務者に対して実施しております。この度、Centogene社とルフトハンザグループが提携したことに伴い、2020年11月12日よりハンブルク空港を出発するルフトハンザドイツ航空の指定されたフライトに搭乗する乗客は、本試薬を用いた高感度抗原検査を受けることができるようになります。
- 今後、Centogene 社がハンブルク空港以外で展開する新型コロナウイルス検査においても高感度抗原検査が採用される予定です。
- 海外渡航者向け唾液PCR検査証明書発行「羽田空港で最短2時間」に
- 学校法人東邦大学、日本空港ビルデング株式会社および東京国際空港ターミナル株式会社、H.U.グループホールディングス株式会社は、東邦大学羽田空港第3ターミナルクリニックにて実施中の唾液PCR検査について、検査体制を拡充し、11月9日より検体採取後「最短2 時間」での陰性証明書発行が可能になります。また、本クリニックのホームページにおいてご提供しているオンライン予約に加え、スマートフォンのPHR(Personal Health Record)アプリに検査結果を通知するサービスを開始します。
- これにより羽田空港における海外渡航者向けPCR 検査の利便性を高め、空の旅を通じた国際間の往来再開に向けて貢献してまいります。
- ※H.U.グループホールディングス株式会社は、傘下のグループ会社が本クリニックよりPCR 検査を受託するとともに、検査結果を確認できるPHR アプリ「ウィズウェルネスTM」を提供しています。
- 【ウィズウェルネスについて】
- ~海外渡航者向け唾液PCR 検査について~
- 検体採取:全日(土日祝日を含む)午前9:00-11:30、午後13:00-17:30
- 証明書発行:全日(土日祝日を含む)午前9:00-11:30、午後13:00-22:00
- 唾液PCR 検査(RT-PCR)
- 38,500 円(税込)(検査料・証明書発行料を含みます。)各種クレジット払い対応
- 詳細は下記のURL よりご確認ください。
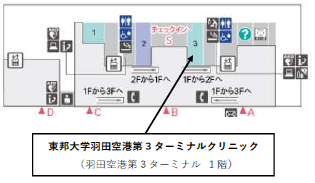
- 〇東邦大学羽田空港第3 ターミナルクリニック
- 〇海外渡航者向け唾液PCR 検査について
- 2020年11月22日・23日の連休における新型コロナウイルスPCR検査体制についてお知らせします。
- 検査項目【0987】新型コロナウイルスRNA 定性は、2020年11月23日(月)の15:00 までに弊社に搬入された検体について、11月22日(日)搬入分と合わせて、11月23日に検査を行います。(11月22日は検査を行いません)
- 至急FAX 分については11月23日(月)検査終了後に報告します。報告書は11 月25 日(水)の報告となります。
- 前鼻腔検体でのPCR検査は7/17より検体採取・輸送マニュアルに追記されています。
- 弊社グループ会社である富士レビオ株式会社(代表取締役社長:藤田 健、本社:東京都新宿区、以下「富士レビオ」)が製造販売する新型コロナウイルス(SARS-CoV-2)の高感度抗原検査試薬(製品名:ルミパルス® SARS-CoV-2 Ag)および迅速抗原検査キット(製品名:エスプライン® SARS-CoV-2)において、検体種別に鼻腔拭い液を追加することが、2020 年 10 月 2 日に厚生労働省より承認されましたのでお知らせいたします。
- エスプラインSARS-CoV-2は2020年5月13日、ルミパルスSARS-CoV-2Ag は 2020年6月19日に製造販売承認を取得し、全国の医療機関等でご採用いただいております。
- この度、検体種別に追加された鼻腔拭い液は、医療従事者の管理下において患者さまご自身が採取することができ、医療従事者の感染リスクが低いことから感染防護対策もサージカルマスク、手袋で足りるとされています※1。検体採取における業務負荷も軽減され、また季節性インフルエンザの流行期を今後迎えることから、診療所等における発熱患者さまへの検査に貢献できるものと考えております。
- 先日、経済産業省より渡航先国の要求に応じた新型コロナウイルス陰性検査証明を円滑に取得するための仕組みである海外渡航者新型コロナウイルス検査センター(TeCOT)を開設するとの発表がありましたが、参加される医療機関様の正式登録が始まりました。申請の際には委託先の衛生検査所等の詳細情報が必要となってきます。弊社、必要書類情報は下記リンクよりご確認ください。
- 2020 年9月 20 日・21 日・22 日の連休における新型コロナウイルス PCR 検査体制についてお知らせします。
- 検査項目【0987】新型コロナウイルス RNA 定性は、2020 年 9 月 21 日(月)の15:00 までに弊社に搬入された検体について、9 月 20 日(日)搬入分と合わせて、9 月 21 日に検査を行います(9 月 20 日・22 日は検査を行いません)。至急 FAX 分については 9 月 21 日(月)検査終了後に報告します。報告書は9月24 日(木)の報告となります。
- 新型コロナウイルス陰性証明書についての要望をたくさんいただいていますのでフォーマットを作成しました。
- 下記リンクファイルは新型コロナウイルスの陰性証明するにあたり、必要な情報をあらかじめ入力しています。
- ワードで作成していますのでご施設様に合った形式に編集してお使いください。
- ※本フォーマットは医療関係者が各種機関に陰性を証明するためのものであって一般の方の使用はお断りいたします。
- 当社のグループ会社で新型コロナウイルスの環境中における拭き取り検査の受託を開始いたしました。
- 当社のグループ会社である株式会社日本食品エコロジー研究所(代表取締役社長:牧野 育也、本社:兵庫県神戸市)と、みらかヴィータス株式会社(代表取締役社長:牧野 育也、本社:東京都世田谷区)は、2020 年 8 月 3 日より、新型コロナウイルス(SARS-CoV-2)の環境中における拭き取り検査(以下「本検査」)の受託を開始いたしましたのでお知らせいたします。
- 本検査は、医療機関や飲食店・宿泊施設等の法人をサービスの対象として想定しております。ドアノブやテーブル、手すり、エレベーターボタン等、人の手が多く触れる箇所を綿棒により拭き取ることによって検体を採取し、同じく当社のグループ会社である合同会社 H.U.グループ中央研究所(職務執行者:小見和也、本社:東京都八王子市)からの技術移管を得て PCR 検査を実施します。
- 当社グループは、これまで臨床検査領域で培った検査技術を応用し、環境中の新型コロナウイルスの拭き取り検査を受託することで、人々の暮らしの安全と感染拡大の抑制に貢献してまいります。
- 鼻咽頭拭い液検体1本で新型コロナウイルス抗原とインフルエンザウイルス抗原の迅速検査が可能です。
- 当社のグループ会社である富士レビオ株式会社は、新型コロナウイルス(SARS-CoV-2)抗原の迅速診断キット「エスプライン®SARS-CoV-2」で用いる検体処理液が、インフルエンザウイルス抗原の迅速診断キット「エスプラインインフルエンザA&B-N」においても使用できることを確認しましたのでお知らせいたします。
- 検査を同一の鼻咽頭拭い液検体で行うことが可能となり、検体採取が1回で済むことから、検体採取時における患者さまの負担軽減および医療従事者の感染リスクを低減することに貢献することができるものと考えております。
- この度、SARS-COV-2抗体の検査項目につきまして検査所要日数を変更いたします
- [実施日]2020年 8月 1日 (土) ご依頼分より変更
- [変更理由]外部委託 (委託先:エスアールエル)より当社にて測定実施へ変更
- *その他、検査基準値等の変更はありません
- 感染の拡大がほぼ終息したと思われていた新型コロナウイルスが再度、流行の兆しを見せており、弊社でもPCR検査受託数が急増しております。試薬の安定受給と検査受託数拡大の為、試薬を変更いたします。
- 尚、本試薬は国立感染症研究所「病原体検出マニュアル 2019-nCoV Ver.2.6」に記載のキット間の比較検討に基づき、国立感染症研究所の方法と同等であると評価された試薬です。
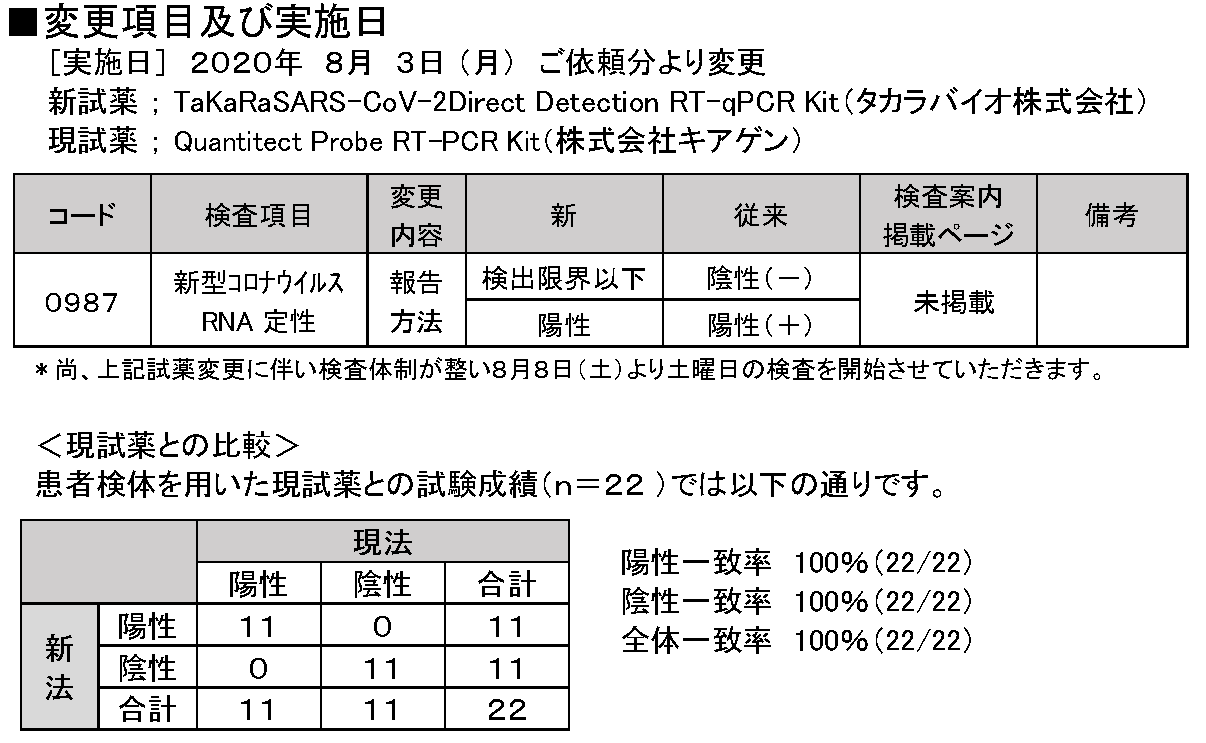
- [ 実施日 ] 2020年 8月 3日 (月) ご依頼分より変更
- 新試薬 ; TaKaRaSARS-CoV-2Direct Detection RT-qPCR Kit(タカラバイオ株式会社)
- 現試薬 ; Quantitect Probe RT-PCR Kit(株式会社キアゲン)
- <現試薬との比較>
- 患者検体を用いた現試薬との試験成績(n=22 )では以下の通りです。
- 陽性一致率 100%(22/22)
- 陰性一致率 100%(22/22)
- 全体一致率 100%(22/22)
- 2020 年7 月23 日~7 月26 日までの期間における新型コロナウイルスPCR 検査体制について
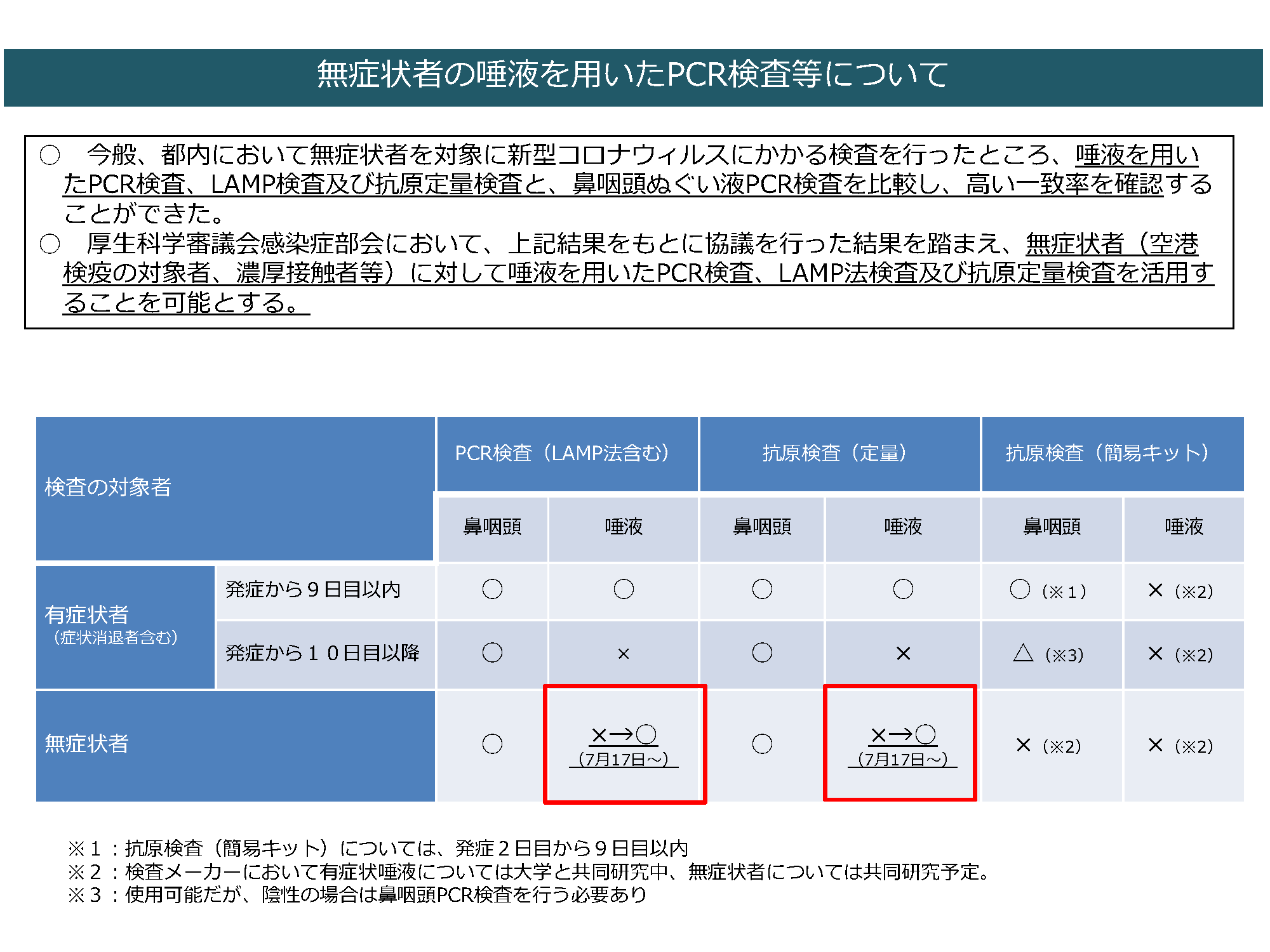
- 厚生労働省は2020年7月17日、新型コロナウイルス感染症の診断に用いるPCR検査および抗原定量検査について、唾液検体を用いた検査の対象を空港検疫の対象者、濃厚接触者などを含む無症状者にも拡大する方針を示しました。
- 出典:厚生労働省「無症状者の唾液を用いたPCR検査等について」
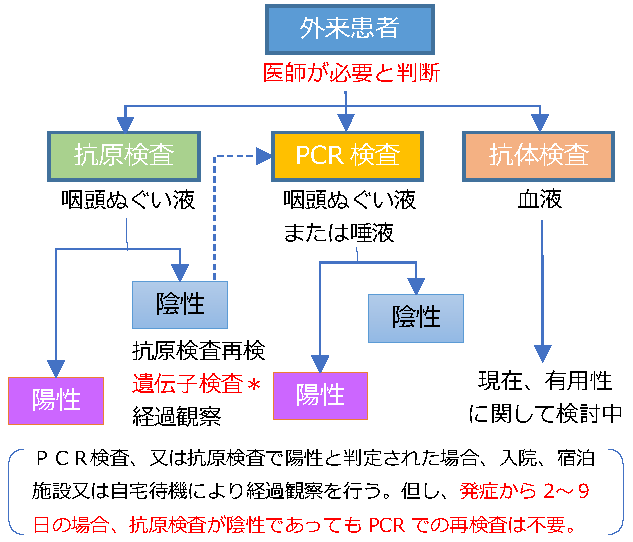
- ~新型コロナウイルス検査の使い分け~
- このたび、唾液を用いた新型コロナウイルス PCR 検査の受託を開始いたしましたのでご案内いたします。
- 弊社ではコロナ禍の早急な終息の為、保険適応外でのPCR 検査も積極的に受託することといたしました。
- 新型コロナウイルスに感染した患者様の早期回復と一刻も早い事態の鎮静化を心よりお祈り申し上げます。
- ~ 保険請求が可能な機関 ~
- a.感染症指定医療機関
- b.a以外の医療機関で感染症法に基づき入院患者が入院している医療機関
- c.帰国者・接触者外来及び帰国者・接触者外来と同様の機能を有する医療機関
- cに該当するものは下記条件を全て満たし、都道府県の認可を受けた施設です。
- ⅰ.感染症を疑う患者とそれ以外の患者が接触しないよう動線が分けられている
- (少なくとも診察室は分けることが望ましい)
- ⅱ.必要な検査体制が確保されている
- ⅲ.適切な感染対策が講じられている
- ・標準予防策に加えて、飛沫予防策及び接触予防策を実施すること
- ・採取された唾液検体を回収する際には、サージカルマスク及び手袋を着用すること。
- *申請については医療機関単体からでも取りまとめ機関(医師会等)からも可能です。
- *保険適応条件として、コロナウイルスを疑い、医師が必要と判断した場合です。
- *健診目的、調査目的での保険適応は出来ません。
- *自費診療のものは上記の申請は必要ありません。
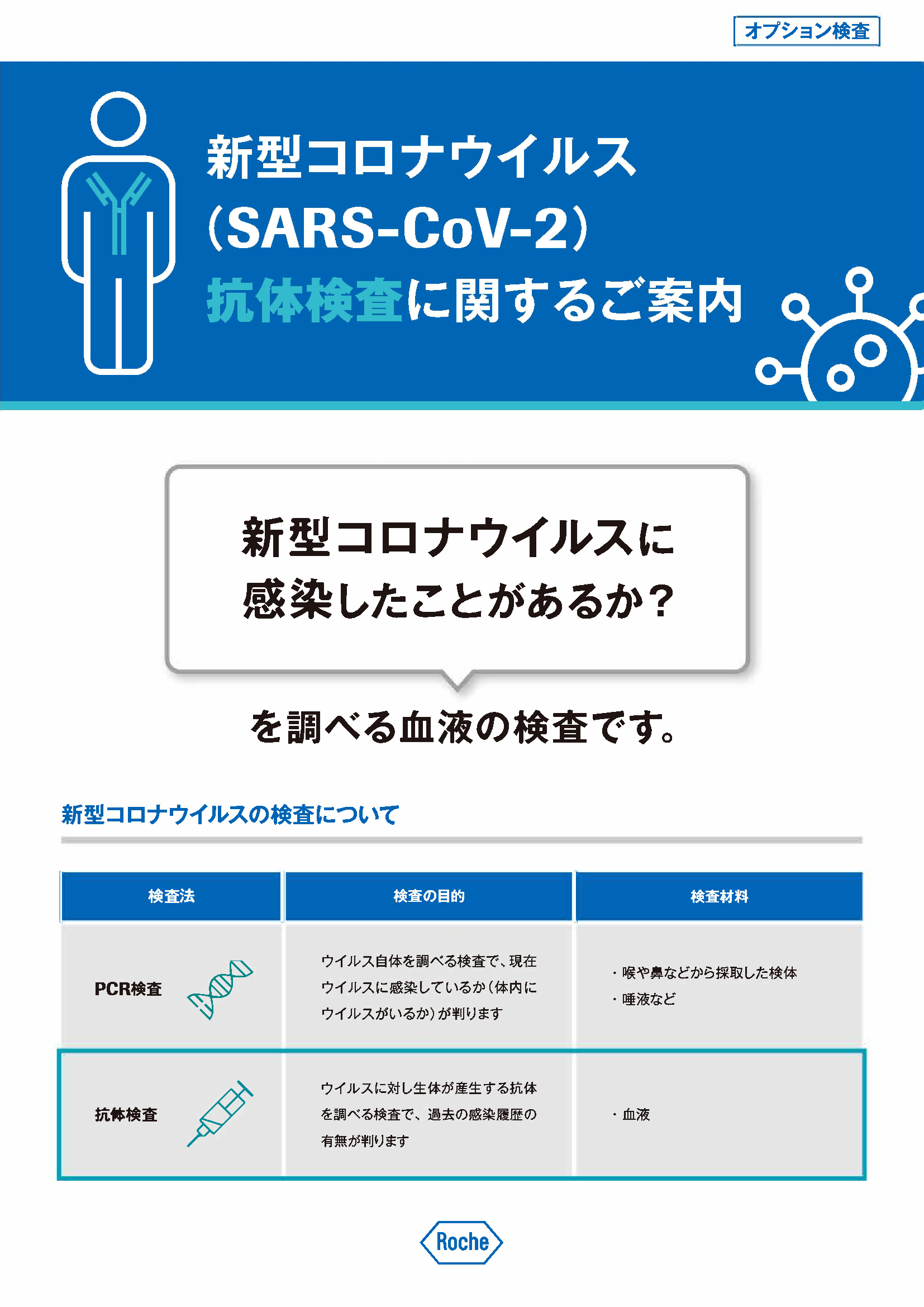
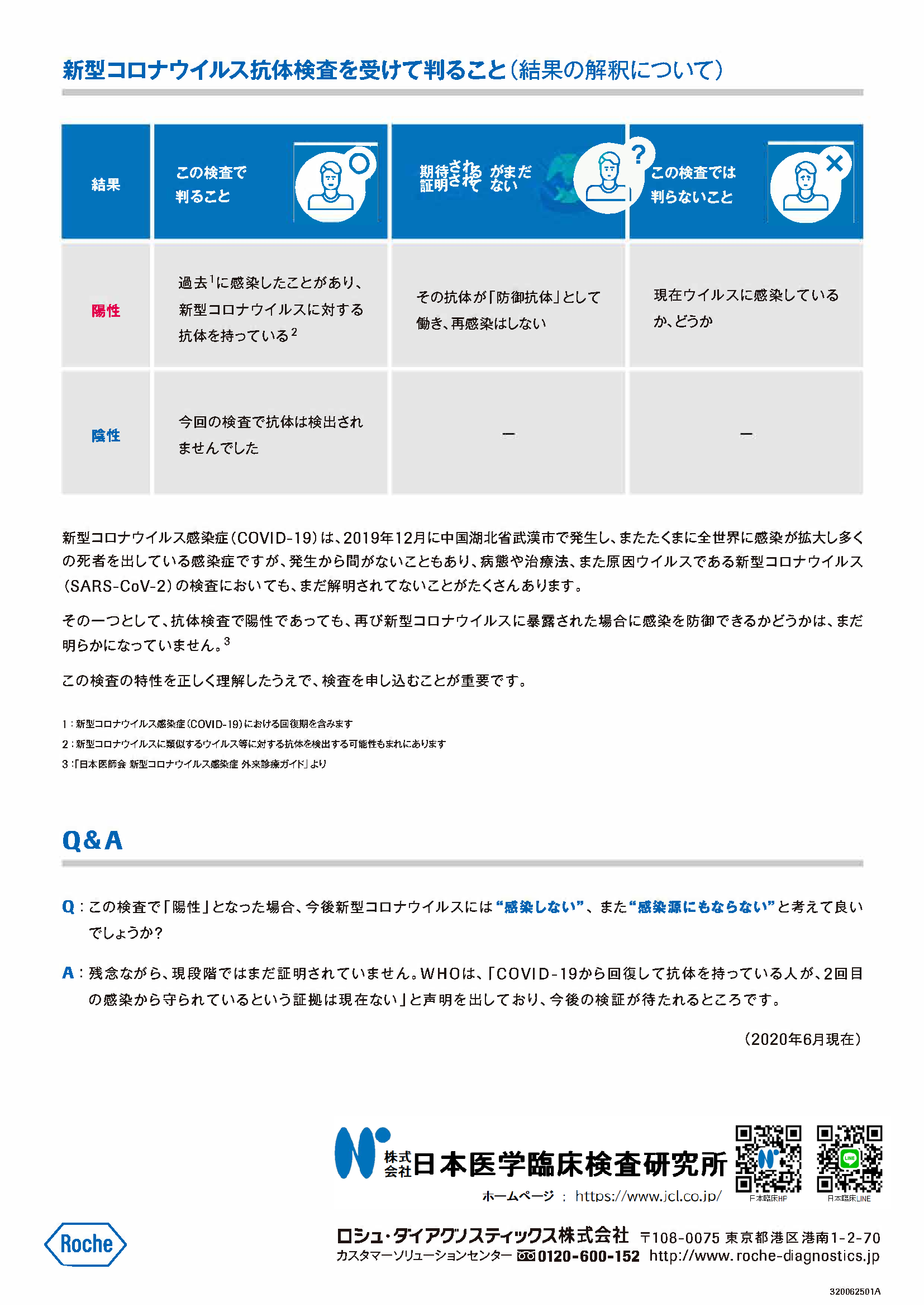
- このたび、新型コロナウイルス抗体検査の受託を開始いたしましたので、ご案内いたします。
- 2020年6月1日時点での保険は未収載です。価格についてはお近くの弊社営業所へご連絡ください。
- 「保医発0513第1号」により下記の検査項目に検査実施料が新設されましたので、ご案内いたします。
- ■ 適用日 令和2年5月13日から適用
- *簡易キットについては弊社でも販売しております。お近くの営業所へお申し付けください。
- GW中の新型コロナウイルス検査受託についてアッセイ日が決定しましたのでお知らせいたします。
- GW期間中は19:00までに搬入されたものを当日受付とさせていただきます。
- (ゆうパックの受け取りは土日祝でも行いますが、アッセイは上記スケジュールとなります。)
- また、報告は過誤防止のため、通常通りの運用とさせていただきたいと考えています。
- 新型コロナウイルスについて現在、検体量が増えており、当初、翌日には報告させていただいていましたが、報告に2~5日の時間をいただいております。ご利用の先生方には大変ご迷惑をおかけすることと存じますが、何卒ご了承賜りますよう宜しくお願い申し上げます。
- 株式会社日本医学臨床検査研究所は、新型コロナウイルス(SARS-CoV-2)の検査を3月6日より臨床検査として受託することとなりましたのでお知らせいたします。
- 弊社は、厚生労働省および国立感染症研究所からの依頼に基づき、これまでも行政検査として本検査を受託してまいりましたが、このたび、帰国者・接触者外来を設置している医療機関等における検査が3月6日に保険適用されることを受け、臨床検査としての受託を開始するものです。
- (*注)検体採取を行った保険医療機関以外の施設へ輸送し検査を委託して実施した場合:1,800点、
- それ以外の場合:1,350点
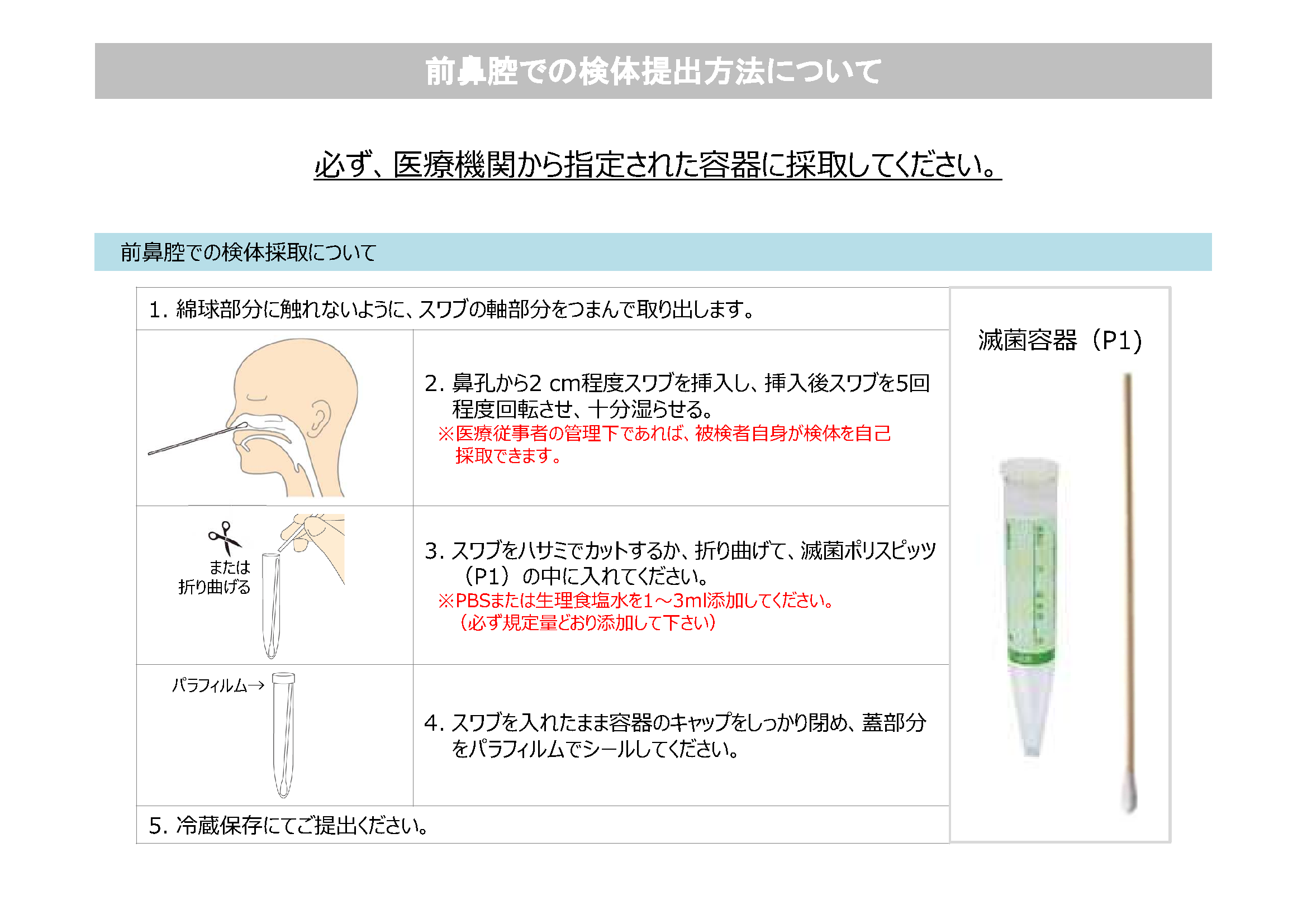
- ・ 鼻咽頭ぬぐい液は、鼻腔用のフロックスワブまたは滅菌綿棒を鼻孔から挿入し、上咽頭を充分に
- 拭い、ウイルス輸送液(VTM/UTM)が入った滅菌スピッツ容器(P1)に入れて下さい。
- ウイルス輸送液が無い場合は、PBS又は生理食塩水で代用して下さい。
- ・ 咽頭ぬぐい液、下気道由来検体(気管吸引液、肺胞洗浄液)も受託可能です。1~2mLを目安に
- ご提出ください。
- ・ 提出容器は、必ず、蓋部分をパラフィルムでシールしてください。
- ・ 本検査方法ではコンタミネーションの影響がより大きくなりますので、検体採取にあたっては
- 取り扱いに十分ご注意ください。他項目との重複依頼は避けてください。
※検査キャパシティを大幅に超える受託があった場合、上記報告日数より遅延する可能性があります。
提出方法等はこちら → “詳細情報表示”
☆☆☆トピックス☆☆☆
■検査使い分けについて(病原体検査の指針) ☜リンクはここをクリックしてください!!
■新型コロナウイルスの消毒・除菌方法について ☜リンクはここをクリックしてください!!
■日本からの渡航・各国の入国制限措置等について ☜リンクはここをクリックしてください!!
~LINE公式アカウントを開設いたしました~
新型コロナウイルス情報、弊社からのお知らせ、最新トピックス、採用情報等の情報をスマホで確認いただけます。
またAI機能を利用した検査項目検索など様々な機能が搭載されています。検査項目案内の代わりにご使用ください。
詳細情報はこちら → ![]() 登録QRコード →
登録QRコード →
| コード | 検査項目 | 採取量(mL) 提出量(mL) |
容器 | 保存 方法 |
所要 日数 |
検査方法 | 基準値 | ||
| 3574 | 新型コロナウイルス核酸検出 (鼻咽頭・鼻腔) |
鼻咽頭・鼻腔 ぬぐい液 |
O3 | 冷蔵 | 2 | PCR (リアルタイムRT-PCR) |
陰性 (-) |
||
| 3590 | 新型コロナウイルス核酸検出 (喀痰・唾液) |
喀痰 2.0 |
L1 |
または O3 |
|||||
| 唾液 1.0 |
L1 |
||||||||
| 0987 | 新型コロナウイルス RNA 定性 |
鼻咽頭・鼻腔 ぬぐい液 |
P1 | ||||||
| 喀痰 2.0 唾液 1.0 |
P1 |
||||||||
|
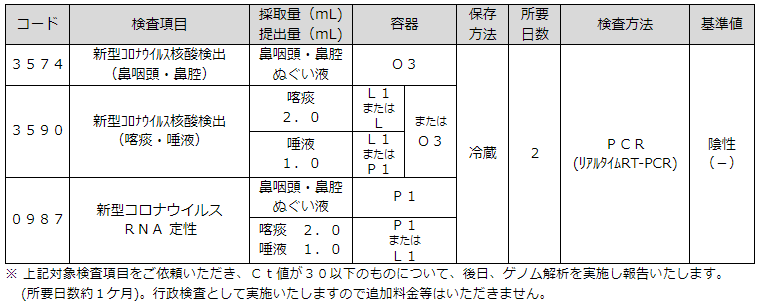
※ 上記対象検査項目をご依頼いただき、Ct値が30以下のものについて、後日、ゲノム解析を実施し報告いたします。 |
|||||||||
▼保険点数詳細内容
|
SARS-CoV-2核酸検出 |
|||
| 検査項目 |
保険点数 |
判断料 |
診療報酬 点数表区分 |
| SARS-CoV-2 核酸検出 |
700点 (350点×2回分) |
微生物学的検査判断料 150点 |
「D023」の10 (HPV核酸検出) |
| 備考 | |||
|
SARS-CoV-2核酸検出は、検査の委託の有無にかかわらず、本区分の「10」HPV核酸検出の所定点数2回分を合算した点数を準用して算定する。なお、採取した検体を、国立感染症研究所が作成した「感染性物質の輸送規則に関するガイダンス2013-2014版」に記載されたカテゴリーBの感染性物質の規定に従って、検体採取を行った保険医療機関以外の施設へ輸送し検査を委託により実施した場合は、検査を実施した施設名を診療報酬明細書の摘要欄に記載すること。 |
|||
|
SARS-CoV-2・インフルエンザ核酸同時検出 |
|||
| 検査項目 |
保険点数 |
判断料 |
診療報酬 点数表区分 |
| SARS-CoV-2・ インフルエンザ 核酸同時検出 |
700点 (350点×2回分) |
微生物学的検査判断料 150点 |
「D023」の10 (HPV核酸検出) |
| 備考 | |||
|
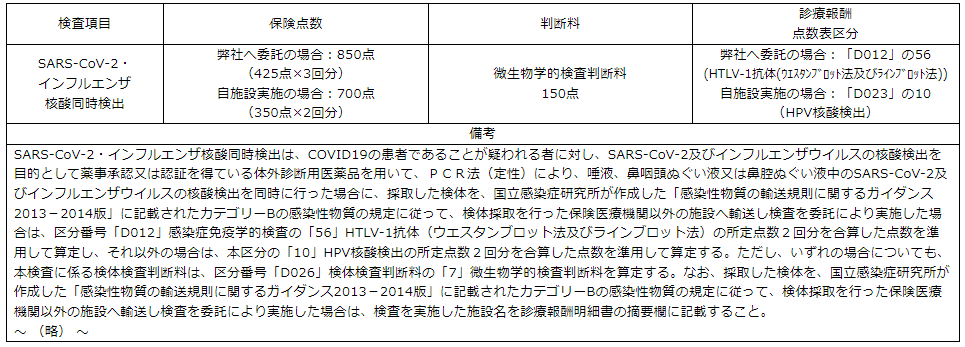
SARS-CoV-2・インフルエンザ核酸同時検出は、COVID-19の患者であることが疑われる者に対し、SARS-CoV-2及びインフルエンザウイルスの核酸検出を目的として薬事承認又は認証を得ている体外診断用医薬品を用いて、PCR法(定性)により、唾液、鼻咽頭ぬぐい液又は鼻腔ぬぐい液中のSARS-CoV-2及びインフルエンザウイルスの核酸検出を同時に行った場合に、検査の委託の有無にかかわらず、本区分の「10」HPV核酸検出の所定点数2回分を合算した点数を準用して算定する。なお、採取した検体を、国立感染症研究所が作成した「感染性物質の輸送規則に関するガイダンス2013-2014版」に記載されたカテゴリーBの感染性物質の規定に従って、検体採取を行った保険医療機関以外の施設へ輸送し検査を委託により実施した場合は、検査を実施した施設名を診療報酬明細書の摘要欄に記載すること。 |
|||
|
SARS-CoV-2抗原検出(定性) |
|||
| 検査項目 |
保険点数 |
判断料 |
診療報酬 点数表区分 |
| SARS-CoV-2 抗原検出(定性) |
300点 (150点×2回分) |
免疫学的検査判断料 144点 |
「D012」の25 (マイコプラズマ抗原定性) |
| 備考 | |||
|
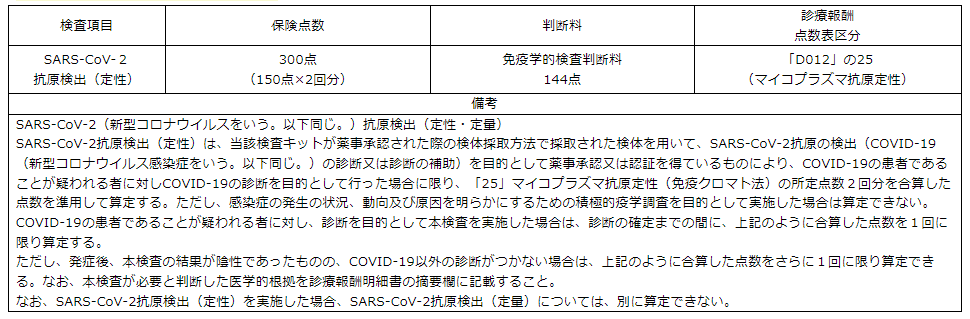
SARS-CoV-2(新型コロナウイルスをいう。以下同じ。)抗原検出(定性・定量) |
|||
|
SARS-CoV-2・インフルエンザウイルス抗原同時検出(定性) |
|||
| 検査項目 |
保険点数 |
判断料 |
診療報酬 点数表区分 |
| SARS-CoV-2・ インフルエンザウイルス 抗原同時検出(定性) |
420点 (210点×2回分) |
免疫学的検査判断料 144点 |
「D012」の39 (単純ヘルペスウイルス抗原定性) |
| 備考 | |||
|
SARS-CoV-2・インフルエンザウイルス抗原同時検出(定性)は、当該検査キットが薬事承認された際の検体採取方法で採取された検体を用いて、SARS-CoV-2抗原及びインフルエンザウイルス抗原の検出を目的として薬事承認又は認証を得ているものにより、COVID-19の患者であることが疑われる者に対しCOVID-19の診断を目的として行った場合に限り、「39」単純ヘルペスウイルス抗原定性(角膜)の所定点数2回分を合算した点数を準用して算定する。ただし、感染症の発生の状況、動向及び原因を明らかにするための積極的疫学調査を目的として実施した場合は算定できない。 |
|||
|
SARS-CoV-2抗原検出(定量) |
|||
| 検査項目 |
保険点数 |
判断料 |
診療報酬 点数表区分 |
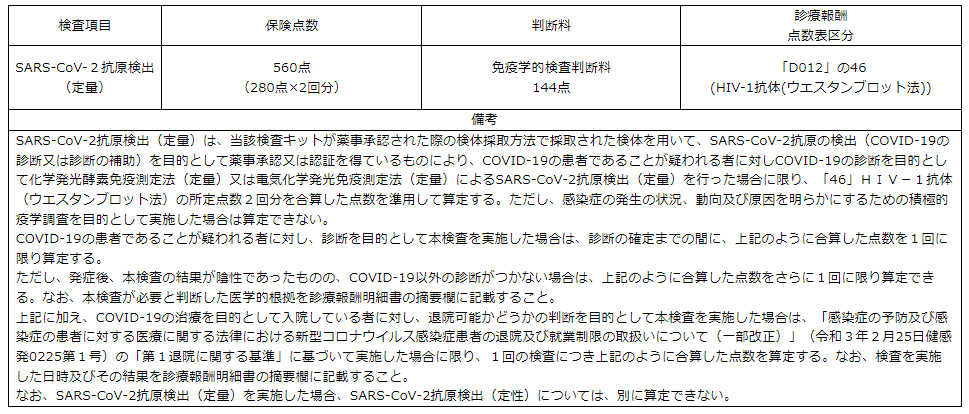
| SARS-CoV-2抗原検出(定量) |
560点 (280点×2回分) |
免疫学的検査判断料 144点 |
「D012」の46 (HIV-1抗体(ウエスタンブロット法)) |
| 備考 | |||
|
SARS-CoV-2抗原検出(定量)は、当該検査キットが薬事承認された際の検体採取方法で採取された検体を用いて、SARS-CoV-2抗原の検出(COVID-19の診断又は診断の補助)を目的として薬事承認又は認証を得ているものにより、COVID-19の患者であることが疑われる者に対しCOVID-19の診断を目的として化学発光酵素免疫測定法(定量)又は電気化学発光免疫測定法(定量)によるSARS-CoV-2抗原検出(定量)を行った場合に限り、「46」HIV-1抗体(ウエスタンブロット法)の所定点数2回分を合算した点数を準用して算定する。ただし、感染症の発生の状況、動向及び原因を明らかにするための積極的疫学調査を目的として実施した場合は算定できない。 |
|||
タイトルをクリックをすると展開されます
NEWS(PCR検査実施料に関するお知らせ)-2022年3月28日-
NR33040案内
2022年3月
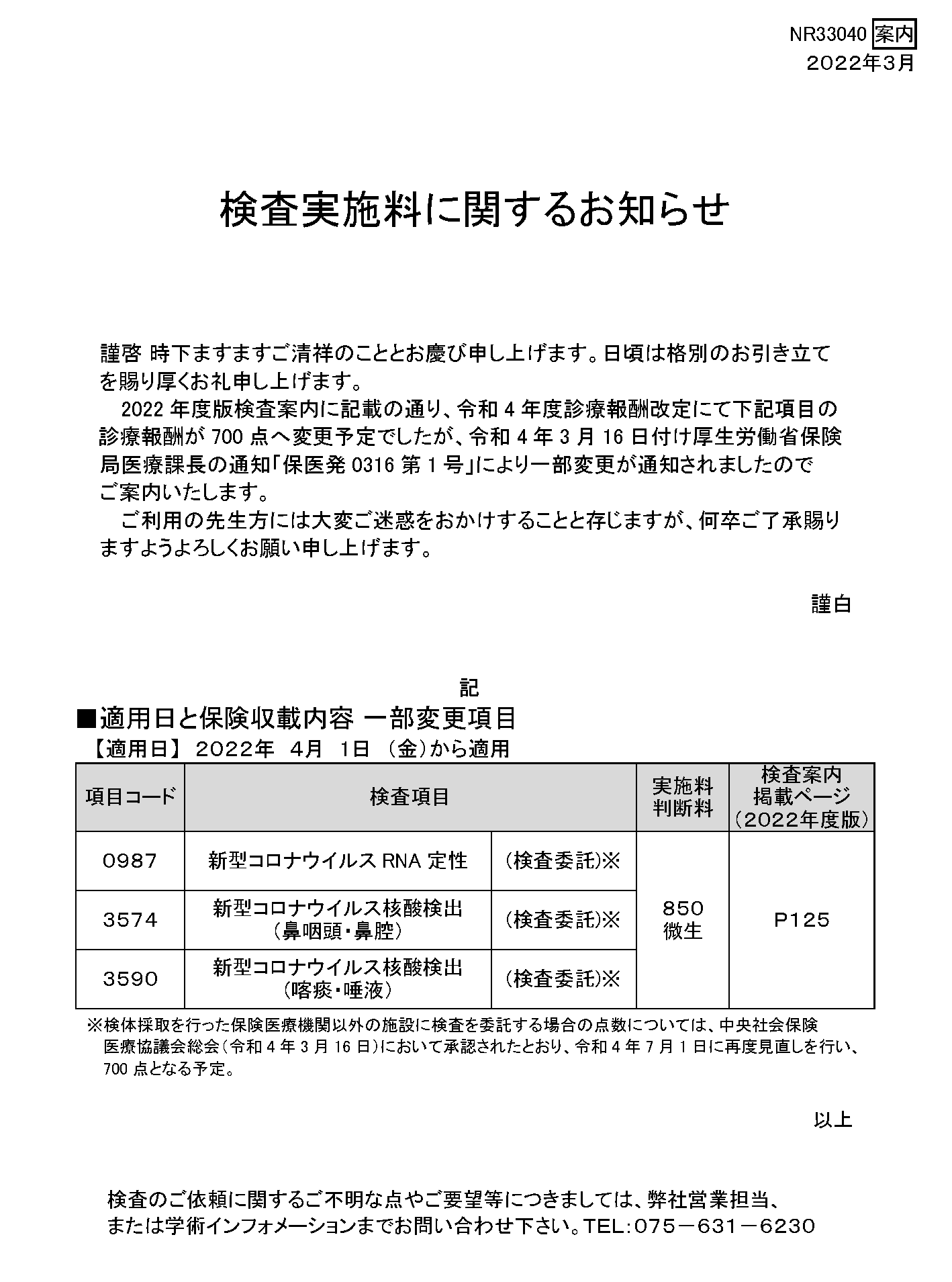
検査実施料に関するお知らせ
■適用日と保険収載内容 一部変更項目
| 項目コード | 検査項目 | 実施料 判断料 |
検査案内 掲載ページ (2022年度版) |
|
| 0987 | 新型コロナウイルス定性 | (検査委託)※ | 850 微生 |
P125 |
| 3574 | 新型コロナウイルス核酸検出 (鼻咽頭・鼻腔) |
(検査委託)※ | ||
| 3590 | 新型コロナウイルス核酸検出 (喀痰・唾液) |
(検査委託)※ | ||
|
※検体採取を行った保険医療機関以外の施設に検査を委託する場合の点数については、中央社会保険医療協議会総会(令和4年3月16日)において承認されたとおり、令和4年7月1日に再度見直しを行い、700点となる予定。 |
||||
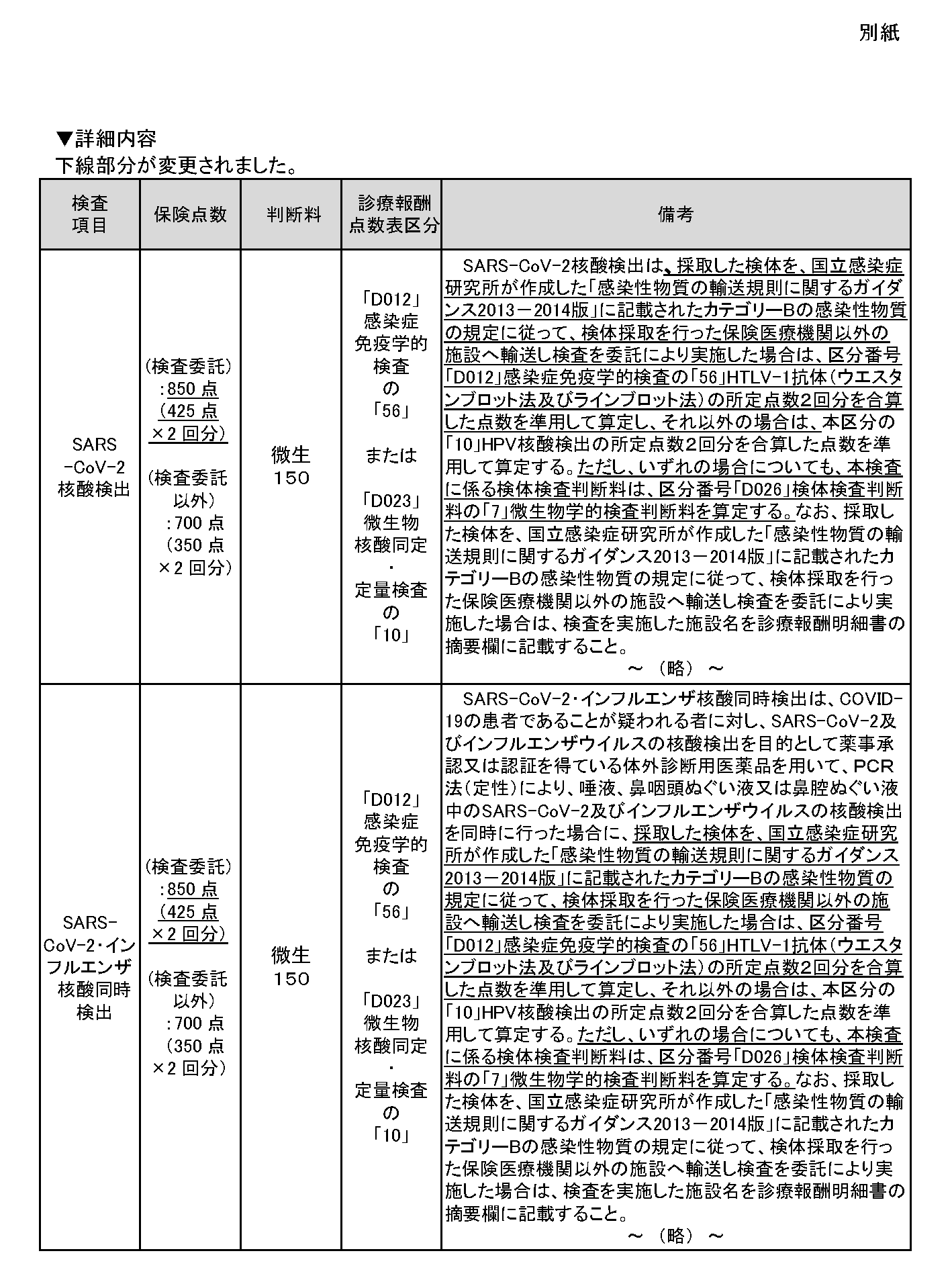
▼詳細内容
下線部分が変更されました。
| 検査 項目 |
保険点数 | 判断料 | 診療報酬 点数表区分 |
備考 |
| SARS-CoV-2核酸検出 | (検査委託) :850点 (425点 ×2回分)
|
微生 150 |
「D012」 感染症 免疫学的 検査 の 「56」 または 「D023」 微生物 核酸同定 ・ 定量検査 の 「10」 |
SARS-CoV-2核酸検出は、採取した検体を、国立感染症研究所が作成した「感染性物質の輸送規則に関するガイダンス2013-2014版」に記載されたカテゴリーBの感染性物質の規定に従って、検体採取を行った保険医療機関以外の施設へ輸送し検査を委託により実施した場合は、区分番号「D012」感染症免疫学的検査の「56」HTLV-1抗体(ウエスタンブロット法及びラインブロット法)の所定点数2回分を合算した点数を準用して算定し、それ以外の場合は、本区分の「10」HPV核酸検出の所定点数2回分を合算した点数を準用して算定する。ただし、いずれの場合についても、本検査に係る検体検査判断料は、区分番号「D026」検体検査判断料の「7」微生物学的検査判断料を算定する。なお、採取した検体を、国立感染症研究所が作成した「感染性物質の輸送規則に関するガイダンス2013-2014版」に記載されたカテゴリーBの感染性物質の規定に従って、検体採取を行った保険医療機関以外の施設へ輸送し検査を委託により実施した場合は、検査を実施した施設名を診療報酬明細書の摘要欄に記載すること。 ~ (略) ~ |
| SARS- CoV-2・イン フルエンザ 核酸同時 検出 |
(検査委託) :850点 (425点 ×2回分)
|
微生 150 |
「D012」 感染症 免疫学的 検査 の 「56」 または 「D023」 微生物 核酸同定 ・ 定量検査 の 「10」 |
SARS-CoV-2・インフルエンザ核酸同時検出は、COVID-19の患者であることが疑われる者に対し、SARS-CoV-2及びインフルエンザウイルスの核酸検出を目的として薬事承認又は認証を得ている体外診断用医薬品を用いて、PCR法(定性)により、唾液、鼻咽頭ぬぐい液又は鼻腔ぬぐい液中のSARS-CoV-2及びインフルエンザウイルスの核酸検出を同時に行った場合に、採取した検体を、国立感染症研究所が作成した「感染性物質の輸送規則に関するガイダンス2013-2014版」に記載されたカテゴリーBの感染性物質の規定に従って、検体採取を行った保険医療機関以外の施設へ輸送し検査を委託により実施した場合は、区分番号「D012」感染症免疫学的検査の「56」HTLV-1抗体(ウエスタンブロット法及びラインブロット法)の所定点数2回分を合算した点数を準用して算定し、それ以外の場合は、本区分の「10」HPV核酸検出の所定点数2回分を合算した点数を準用して算定する。ただし、いずれの場合についても、本検査に係る検体検査判断料は、区分番号「D026」検体検査判断料の「7」微生物学的検査判断料を算定する。なお、採取した検体を、国立感染症研究所が作成した「感染性物質の輸送規則に関するガイダンス2013-2014版」に記載されたカテゴリーBの感染性物質の規定に従って、検体採取を行った保険医療機関以外の施設へ輸送し検査を委託により実施した場合は、検査を実施した施設名を診療報酬明細書の摘要欄に記載すること。 ~ (略) ~ |
タイトルをクリックをすると展開されます
NEWS(年末年始の新型コロナウイルス検査受託について)-2021年12月1日-
|
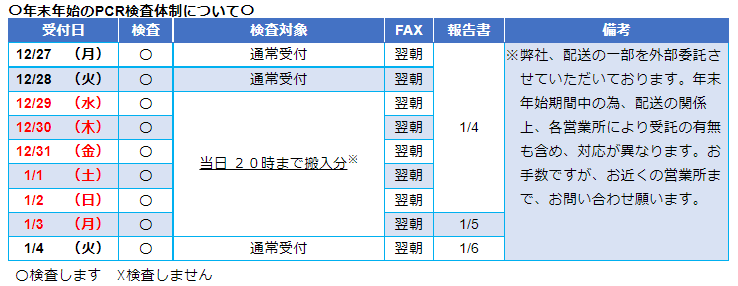
〇年末年始のPCR検査体制について〇 |
||||||
|
受付日 |
検査 |
検査対象 |
FAX |
報告書 |
備考 |
|
| 12/27 | (月) | 〇 | 通常受付 | 翌朝 | 1/4 |
※弊社、配送の一部を外部委託させていただいております。年末年始期間中の為、配送の関係上、各営業所により受託の有無も含め、対応が異なります。お手数ですが、お近くの営業所まで、お問い合わせ願います。 |
| 12/28 | (火) | 〇 | 通常受付 | 翌朝 | ||
| 12/29 | (水) | 〇 | 当日 20時まで搬入分※ | 翌朝 | ||
| 12/30 | (木) | 〇 | 翌朝 | |||
| 12/31 | (金) | 〇 | 翌朝 | |||
| 1/1 | (土) | 〇 | 翌朝 | |||
| 1/2 | (日) | 〇 | 翌朝 | |||
| 1/3 | (月) | 〇 | 翌朝 | 1/5 | ||
| 1/4 | (火) | 〇 | 通常受付 | 翌朝 | 1/6 | |
|
〇検査します ☓検査しません |
||||||
タイトルをクリックをすると展開されます
NEWS(変異株スクリーニング検査受託中止について)-2021年10月15日-
NR33021中止
2021年10月
検査受託中止のお知らせ
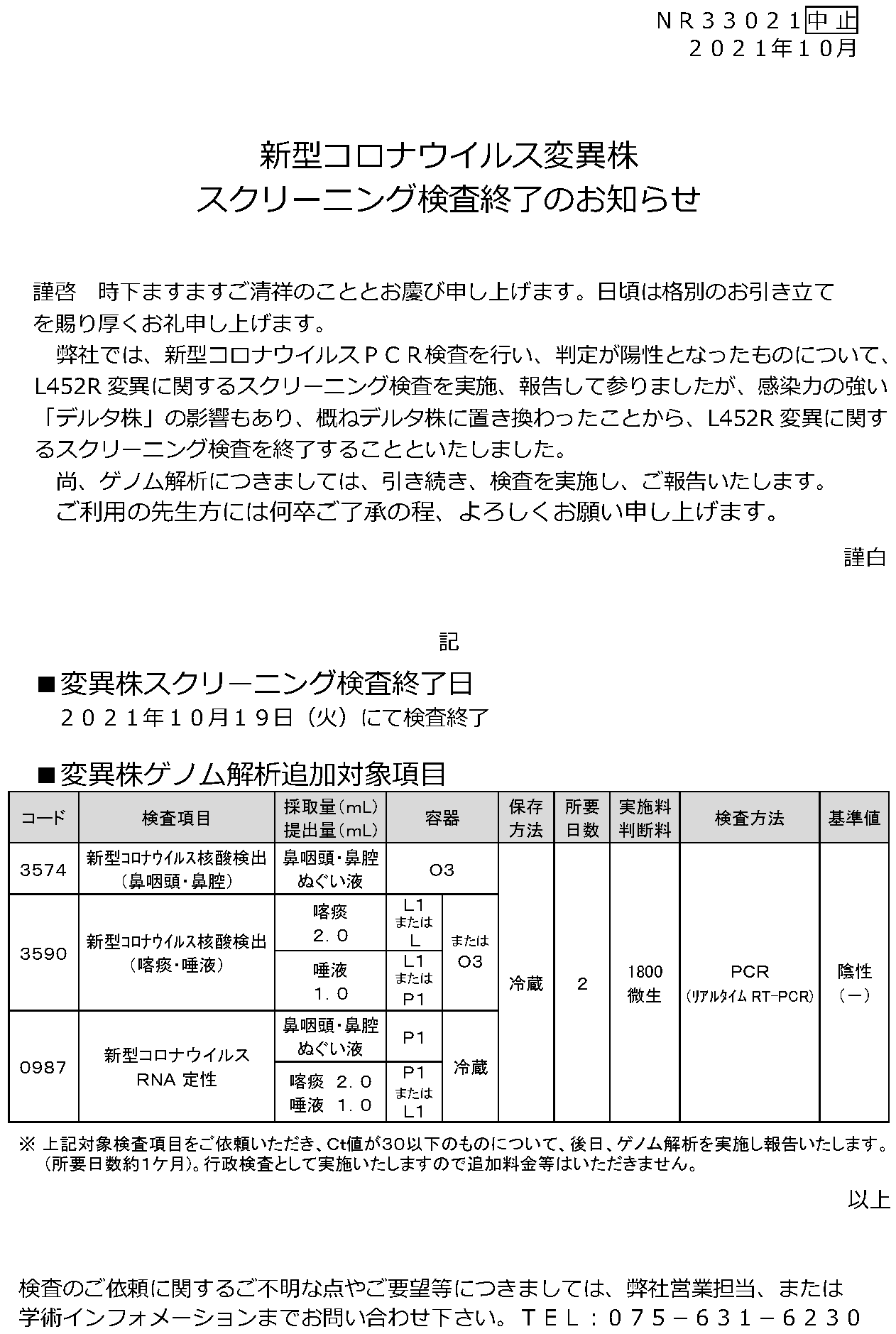
謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを賜り
厚くお礼申し上げます。
弊社では、新型コロナウイルスPCR検査を行い、判定が陽性となったものについて、
L452R 変異に関するスクリーニング検査を実施、報告して参りましたが、感染力の強い
「デルタ株」の影響もあり、概ねデルタ株に置き換わったことから、L452R 変異に関す
るスクリーニング検査を終了することといたしました。
尚、ゲノム解析につきましては、引き続き、検査を実施し、ご報告いたします。
ご利用の先生方には何卒ご了承の程、よろしくお願い申し上げます。
謹白
記
■ 変異株スクリーニング検査終了日
[実施日] 2021年 10月 19日(火)にて検査終了
■ 変異株ゲノム解析追加対象項目
| コード | 検査項目 | 採取量(mL) 提出量(mL) |
容器 | 保存 方法 |
所要 日数 |
実施料 判断料 |
検査方法 | 基準値 | |
| 3574 | 新型コロナウイルス核酸検出 (鼻咽頭・鼻腔) |
鼻咽頭・鼻腔 ぬぐい液 |
O3 | 冷蔵 | 2 | 1800 微生 |
PCR (リアルタイムRT-PCR) |
陰性 (-) |
|
| 3590 | 新型コロナウイルス核酸検出 (喀痰・唾液) |
喀痰 2.0 |
L1 |
または O3 |
|||||
| 唾液 1.0 |
L1 |
||||||||
| 0987 | 新型コロナウイルス RNA 定性 |
鼻咽頭・鼻腔 ぬぐい液 |
P1 | 冷蔵 | |||||
| 喀痰 2.0 唾液 1.0 |
P1 |
||||||||
|
※ 上記対象検査項目をご依頼いただき、Ct値が30以下のものについて、後日、ゲノム解析を実施し報告いたします。 |
|||||||||
タイトルをクリックをすると展開されます
NEWS(お盆期間中の検査受託について)-2021年7月26日-
|
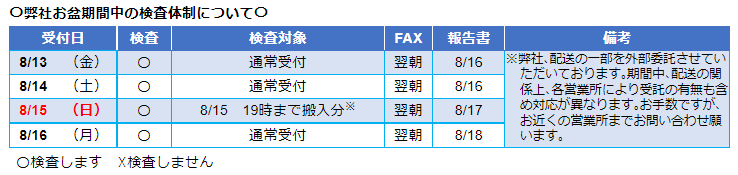
〇弊社お盆期間中の検査体制について〇 |
||||||
|
受付日 |
検査 |
検査対象 |
FAX |
報告書 |
備考 |
|
| 8/13 | (金) | 〇 | 通常受付 | 翌朝 | 8/16 |
※弊社、配送の一部を外部委託させていただいております。期間中、配送の関係上、各営業所により受託の有無も含め対応が異なります。お手数ですが、お近くの営業所までお問い合わせ願います。 |
| 8/14 | (土) | 〇 | 通常受付 | 翌朝 | 8/16 | |
| 8/15 | (日) | 〇 | 8/15 19時まで搬入分※ | 翌朝 | 8/17 | |
| 8/16 | (月) | 〇 | 通常受付 | 翌朝 | 8/18 | |
|
〇検査します ☓検査しません |
||||||
タイトルをクリックをすると展開されます
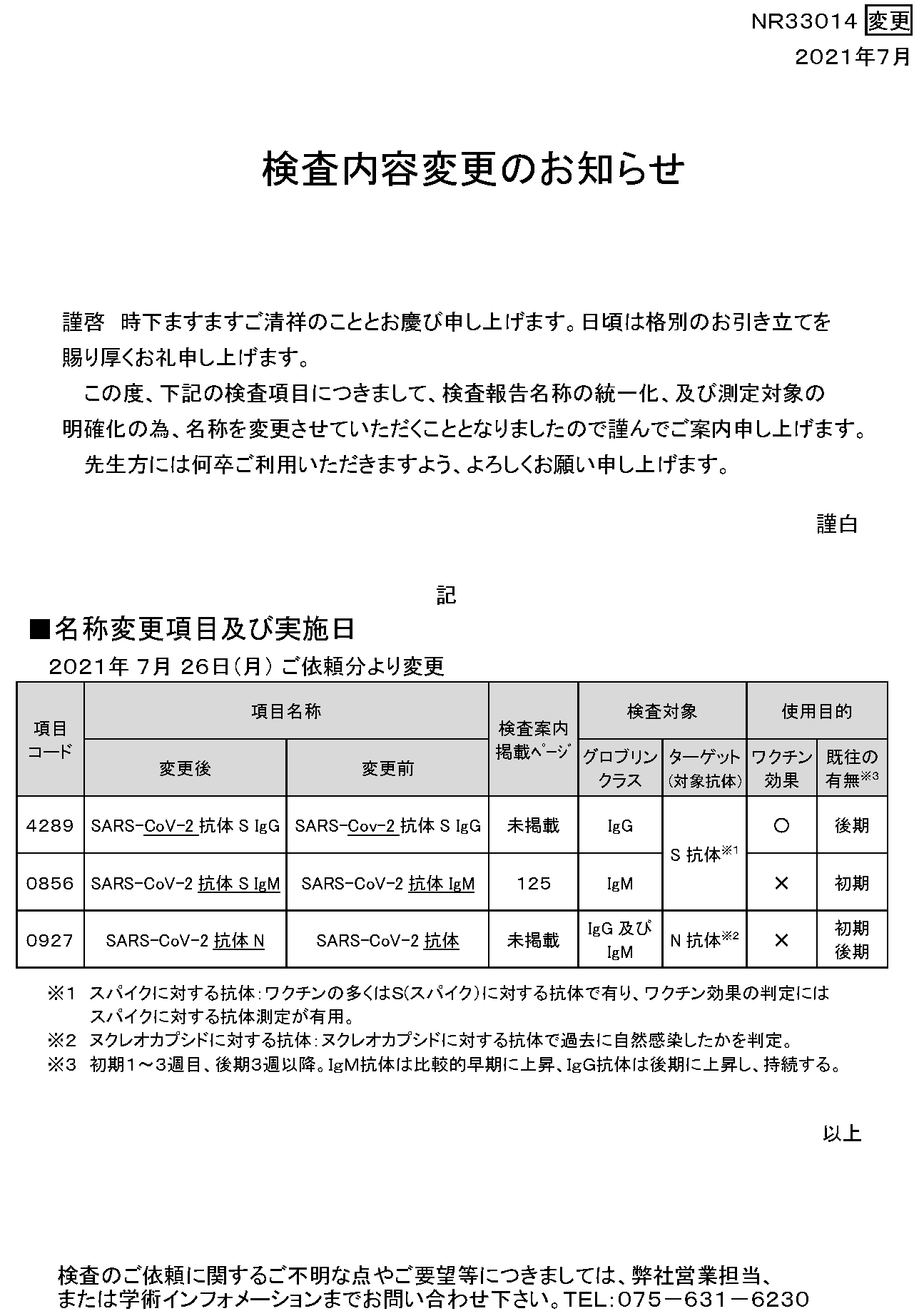
NEWS(SARS-CoV2抗体等 項目名称変更のお知らせ)-2021年7月20日-
NR33014変更
2021年7月
検査内容変更のお知らせ
謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを賜り
厚くお礼申し上げます。
この度、下記の検査項目につきまして、検査報告名称の統一化、及び測定対象の明確化
の為、名称を変更させていただくこととなりましたので謹んでご案内申し上げます。
先生方には何卒ご利用いただきますよう、よろしくお願い申し上げます。
謹白
記
■名称変更項目及び実施日
2021年 7月 26日(月) ご依頼分より変更
|
項目
コード |
項目名称
|
検査案内
掲載ページ |
検査対象
|
使用目的
|
|||
|
変更後
|
変更前
|
グロブリン
クラス |
ターゲット
(対象抗体) |
ワクチン
効果判定 |
既往の
有無※3 |
||
|
4289
|
SARS-CoV-2 抗体 S IgG
|
SARS-Cov-2 抗体 S IgG
|
未掲載
|
IgG
|
S抗体※1
|
○
|
後期
|
|
0856
|
SARS-CoV-2 抗体 S IgM
|
SARS-CoV-2 抗体 IgM
|
125
|
IgM
|
✕
|
初期
|
|
|
0927
|
SARS-CoV-2 抗体 N
|
SARS-CoV-2 抗体
|
未掲載
|
IgG及びIgM
|
N抗体※2
|
✕
|
初期
後期 |
に対する抗体測定が有用。
タイトルをクリックをすると展開されます
NEWS(オリンピック閉会式前後の検査受託について)-2021年7月12日-
|
〇弊社オリンピック期間中の検査体制について〇 |
||||||
|
<オリンピック閉会式前後> |
||||||
|
受付日 |
検査 |
検査対象 |
FAX |
報告書 |
備考 |
|
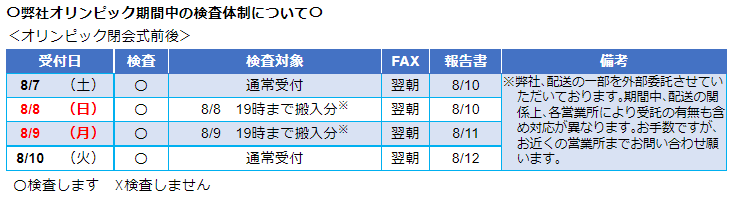
| 8/7 | (土) | 〇 | 通常受付 | 翌朝 | 8/10 |
※弊社、配送の一部を外部委託させていただいております。期間中、配送の関係上、各営業所により受託の有無も含め対応が異なります。お手数ですが、お近くの営業所までお問い合わせ願います。 |
| 8/8 | (日) | 〇 | 8/8 19時まで搬入分※ | 翌朝 | 8/10 | |
| 8/9 | (月) | 〇 | 8/9 19時まで搬入分※ | 翌朝 | 8/11 | |
| 8/10 | (火) | 〇 | 通常受付 | 翌朝 | 8/12 | |
|
〇検査します ☓検査しません |
||||||
タイトルをクリックをすると展開されます
NEWS(オリンピック開会式前後の検査受託について)-2021年7月1日-
|
〇弊社オリンピック期間中の検査体制について〇 |
||||||
|
<オリンピック開会式前後> |
||||||
|
受付日 |
検査 |
検査対象 |
FAX |
報告書 |
備考 |
|
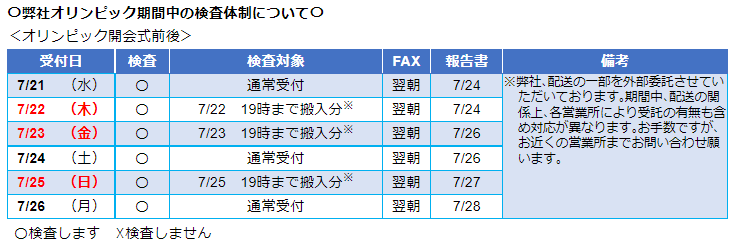
| 7/21 | (水) | 〇 | 通常受付 | 翌朝 | 7/24 |
※弊社、配送の一部を外部委託させていただいております。期間中、配送の関係上、各営業所により受託の有無も含め対応が異なります。お手数ですが、お近くの営業所までお問い合わせ願います。 |
| 7/22 | (木) | 〇 | 7/22 19時まで搬入分※ | 翌朝 | 7/24 | |
| 7/23 | (金) | 〇 | 7/23 19時まで搬入分※ | 翌朝 | 7/26 | |
| 7/24 | (土) | 〇 | 通常受付 | 翌朝 | 7/26 | |
| 7/25 | (日) | 〇 | 7/25 19時まで搬入分※ | 翌朝 | 7/27 | |
| 7/26 | (月) | 〇 | 通常受付 | 翌朝 | 7/28 | |
|
〇検査します ☓検査しません |
||||||
タイトルをクリックをすると展開されます
NEWS(新型コロナ変異株解析 検査対象追加)-2021年6月28日-
■SARS-COV2変異株とは → 変異株とは
NR33009変更
2021年6月
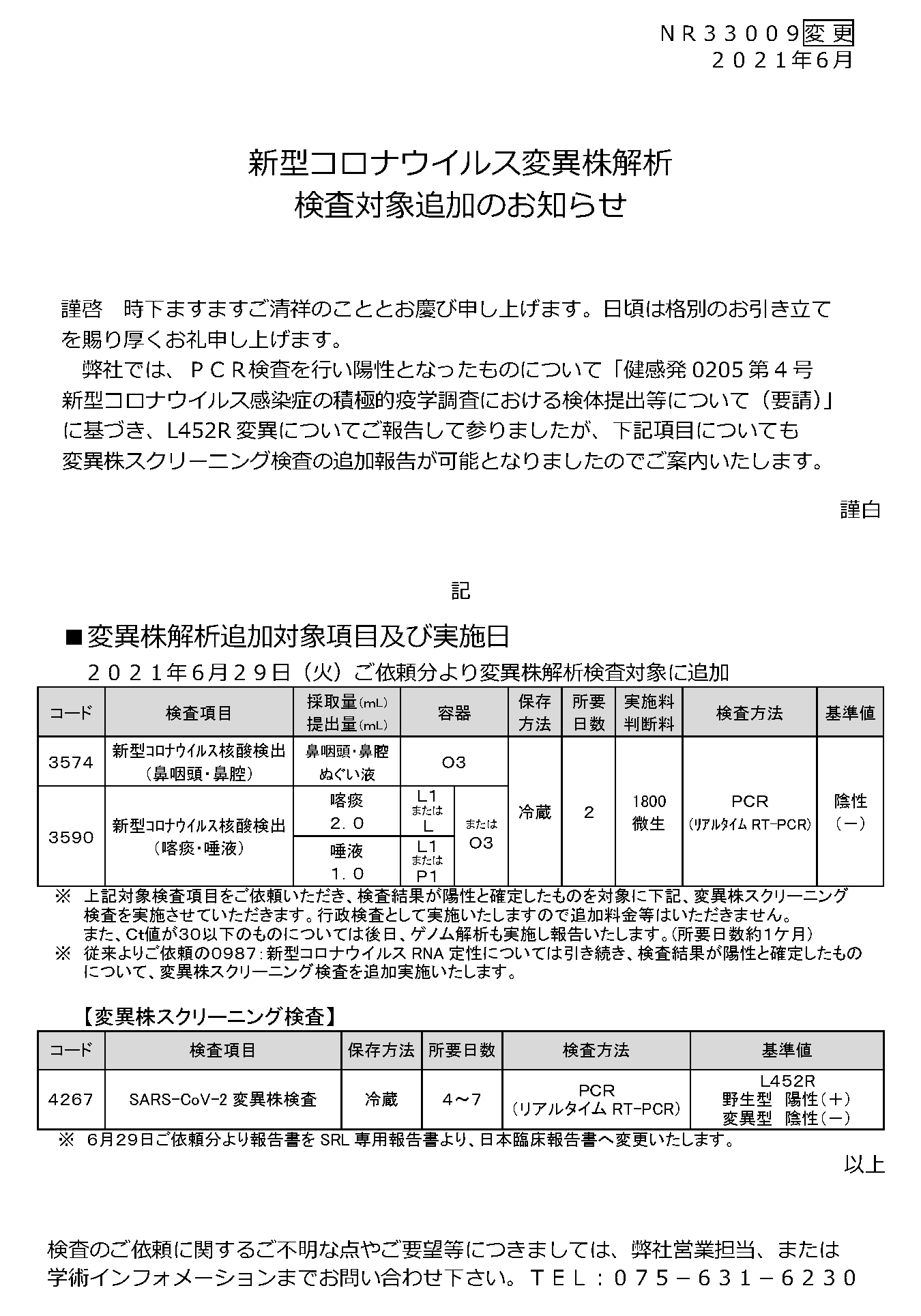
新型コロナウイルス変異株解析
検査対象追加のお知らせ
謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを
賜り厚くお礼申し上げます。
弊社では、PCR検査を行い陽性となったものについて「健感発0205第4号
新型コロナウイルス感染症の積極的疫学調査における検体提出等について(要請)」
に基づき、L452R変異についてご報告して参りましたが、下記項目についても
変異株スクリーニング検査の追加報告が可能となりましたのでご案内いたします。
謹白
記
■変更内容及び実施日
|
コード
|
検査項目
|
採取量(mL)
提出量(mL) |
容器
|
保存
方法 |
所要
日数 |
実施料
判断料 |
検査方法
|
基準値
|
|
|
3574
|
新型コロナウイルス核酸検出
(鼻咽頭・鼻腔) |
鼻咽頭・鼻腔
ぬぐい液 |
O3
|
冷蔵
|
2
|
1800
微生 |
PCR
(リアルタイムRT-PCR) |
陰性
(-) |
|
|
3590
|
新型コロナウイルス核酸検出
(喀痰・唾液) |
喀痰
2.0 |
L1
または L |
または
O3 |
|||||
|
唾液
1.0 |
L1
または P1 |
||||||||
※1 検査を実施させていただきます。行政検査として実施いたしますので追加料金等はいただきません。
※1 また、Ct値が30以下のものについては後日、ゲノム解析も実施し報告いたします。(所要日数約1ケ月)
※2 従来よりご依頼の0987:新型コロナウイルスRNA定性については引き続き、検査結果が陽性と確定したもの
※2 について、変異株スクリーニング検査を追加実施いたします。
【変異株スクリーニング検査】
| コード | 検査項目 | 保存方法 | 所要日数 | 検査方法 | 基準値 | 報告書 |
| 4267 | SARS-CoV-2変異株検査 | 冷蔵 | 4~7 |
PCR
(リアルタイムRT-PCR) |
L452
野生型 陽性(+) 変異型 陰性(-) |
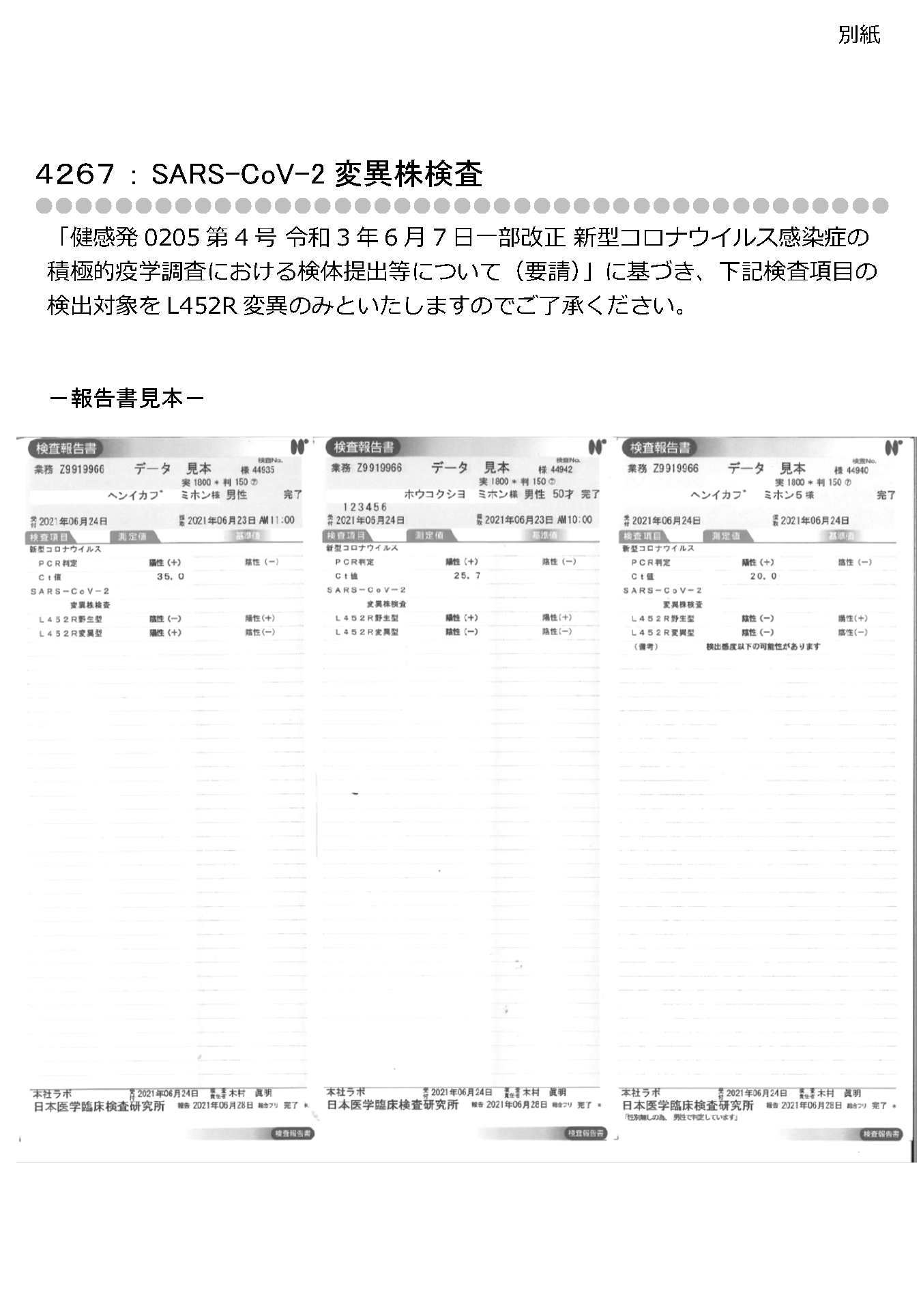
下記見本 |
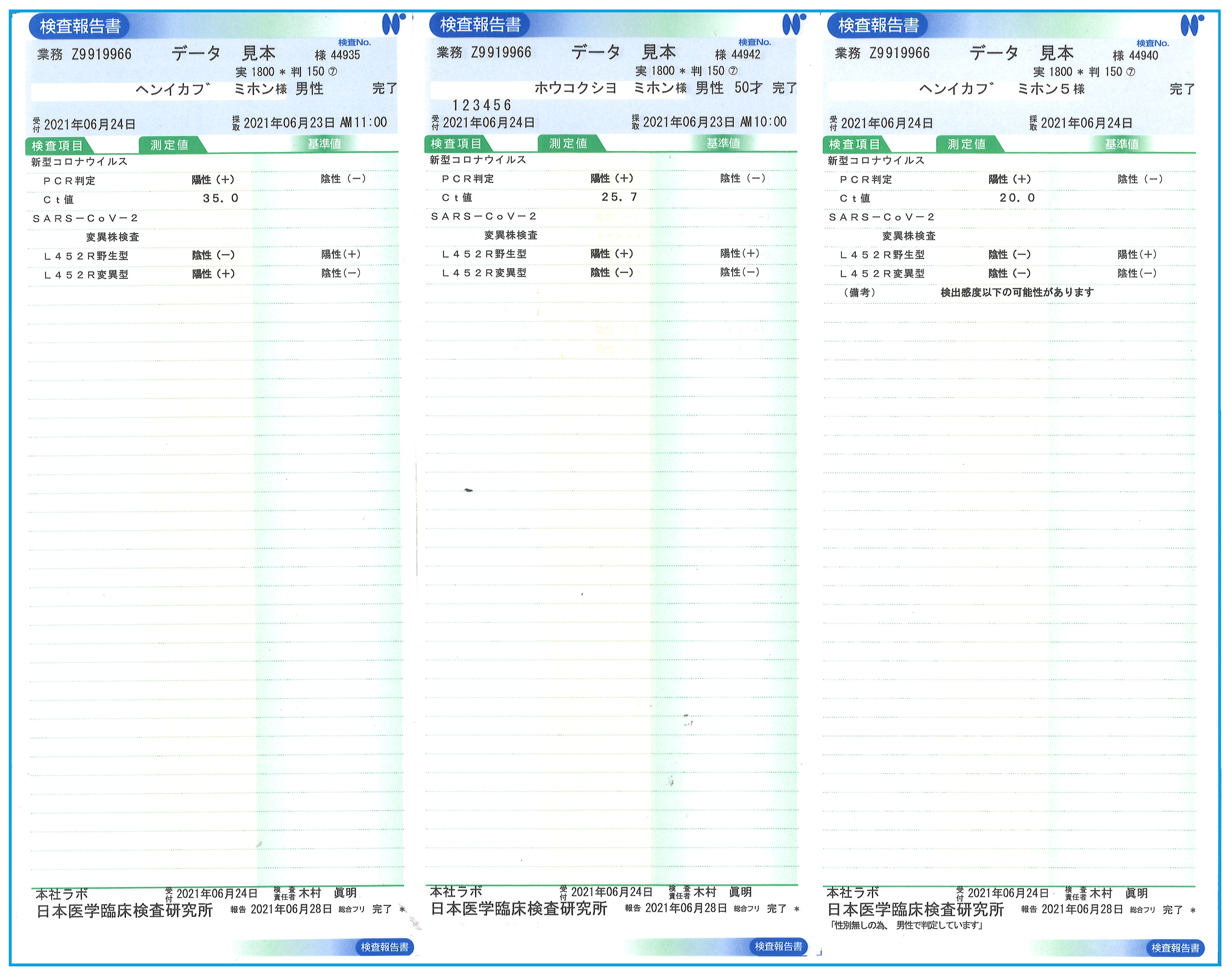
4267 : SARS-CoV-2変異株検査
-報告書見本-
タイトルをクリックをすると展開されます
NEWS(新型コロナ変異株解析 検出対象変更)-2021年6月16日-
■SARS-COV2変異株とは → 変異株とは
NR33008変更
2021年6月
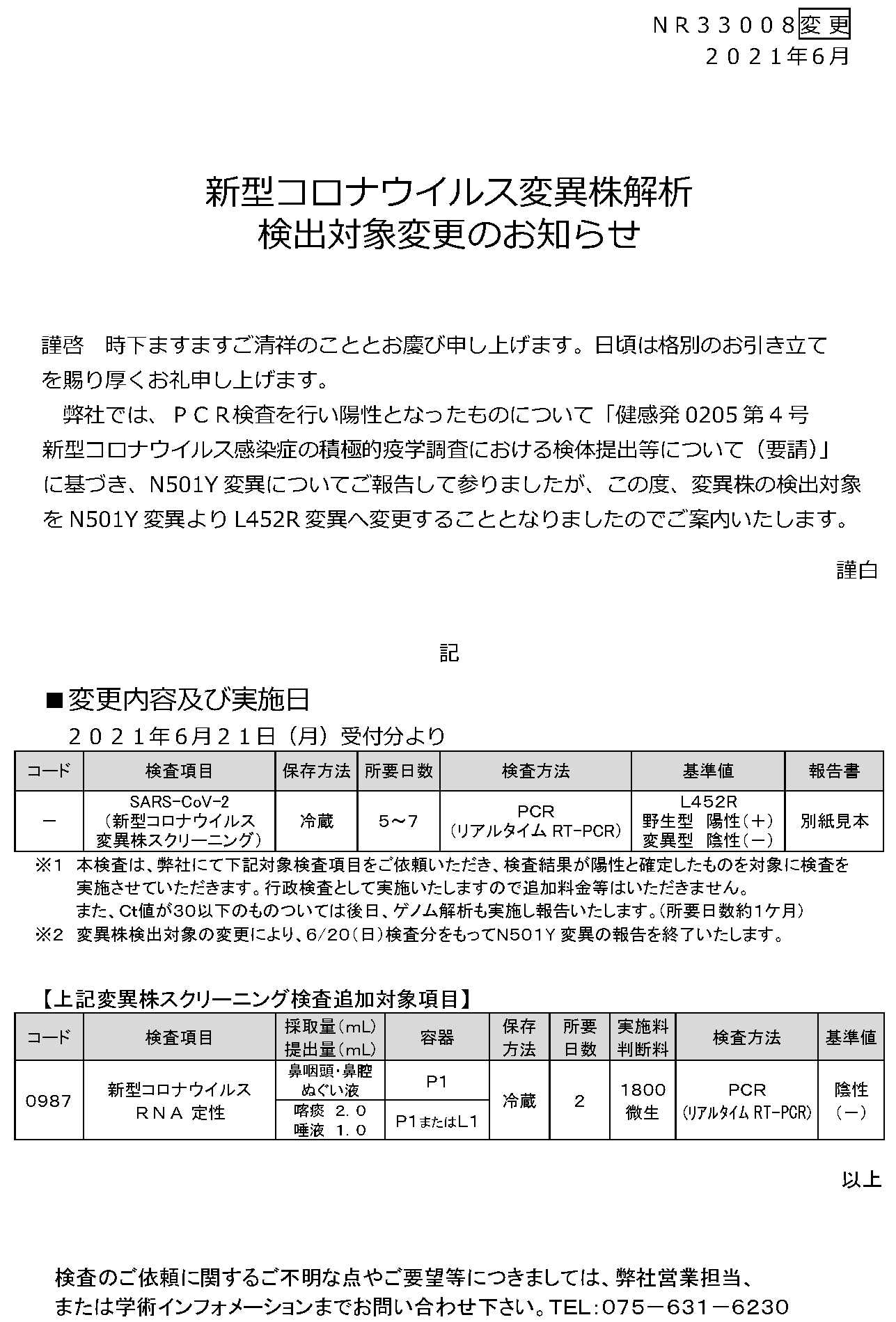
新型コロナウイルス変異株解析
検出対象変更のお知らせ
謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを
賜り厚くお礼申し上げます。
弊社では、PCR検査を行い陽性となったものについて「健感発0205第4号
新型コロナウイルス感染症の積極的疫学調査における検体提出等について(要請)」
に基づき、N501Y変異についてご報告して参りましたが、この度、変異株の検出対象
をN501Y変異よりL452R変異へ変更することとなりましたのでご案内いたします。
謹白
記
■変更内容及び実施日
| コード | 検査項目 | 保存方法 | 所要日数 | 検査方法 | 基準値 | 報告書 |
| - |
SARS-CoV-2
(新型コロナウイルス 変異株スクリーニング) |
冷蔵 | 5~7 |
PCR
(リアルタイムRT-PCR) |
L452
野生型 陽性(+) 変異型 陰性(-) |
別紙見本 |
※1 実施させていただきます。行政検査として実施いたしますので追加料金等はいただきません。
※1 また、Ct値が30以下のものついては後日、ゲノム解析も実施し報告いたします。(所要日数約1ケ月)
※2 変異株検出対象の変更により、6/20(日)検査分をもってN501Y変異の報告を終了いたします。
【上記変異株スクリーニング検査追加対象項目】
| コード | 検査項目 |
採取量(mL)
提出量(mL) |
容器 |
保存
方法 |
所要
日数 |
実施料
判断料 |
検査方法 | 基準値 |
| 0987 |
新型コロナウイルス
RNA定性 |
鼻咽頭・鼻腔
ぬぐい液 |
P1 | 冷蔵 | 2 |
1800
微生 |
PCR
(リアルタイムRT-PCR) |
陰性
(-) |
|
喀痰 2.0
唾液 1.0 |
P1
またはL1 |
タイトルをクリックをすると展開されます
NEWS(SARS-Cov2抗体S IgG 受託開始のお知らせ)-2021年6月7日-
■PDFのダウンロードはこちら →
NR33006案内
2021年6月
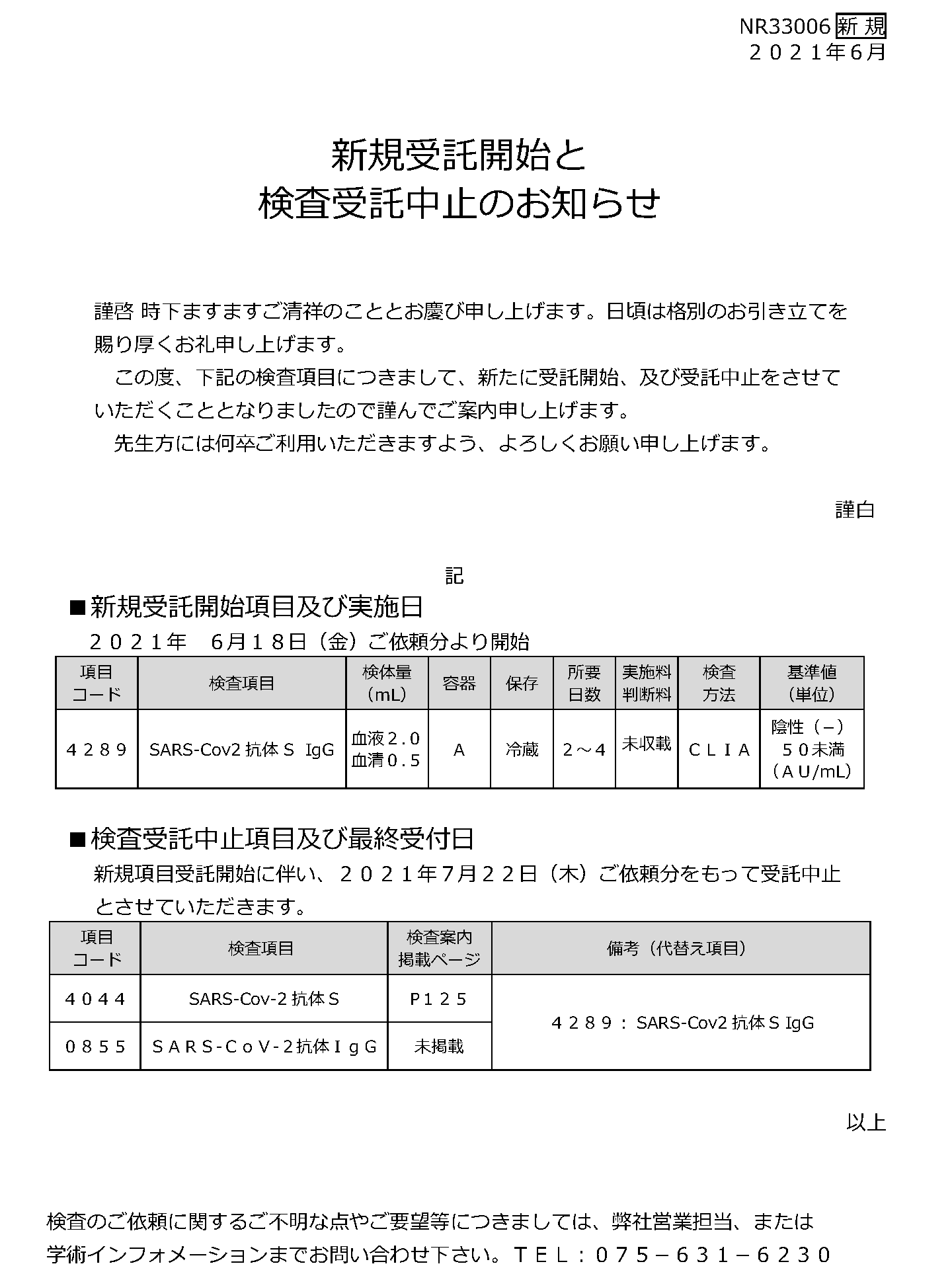
新規受託開始と
検査受託中止のお知らせ
■新規受託開始項目及び実施日
| 項目 コード |
検査項目 | 検体量 (mL) |
容器 | 保存 | 所要 日数 |
実施料 判断料 |
検査 方法 |
基準値 (単位) |
| 4289 | SARS-Cov2抗体S IgG | 血液2.0 血清0.5 |
A | 冷蔵 | 2~4 | 未収載 | CLIA | 陰性(-) 50未満 (AU/mL) |
■検査受託中止項目及び最終受付日
とさせていただきます。
| 項目 コード |
検査項目 | 検査案内 掲載ページ |
備考(代替え項目) |
| 4044 | SARS-Cov-2抗体S | P125 | 4289: SARS-Cov2抗体S IgG |
| 0855 | SARS-CoV-2抗体IgG | 未掲載 |
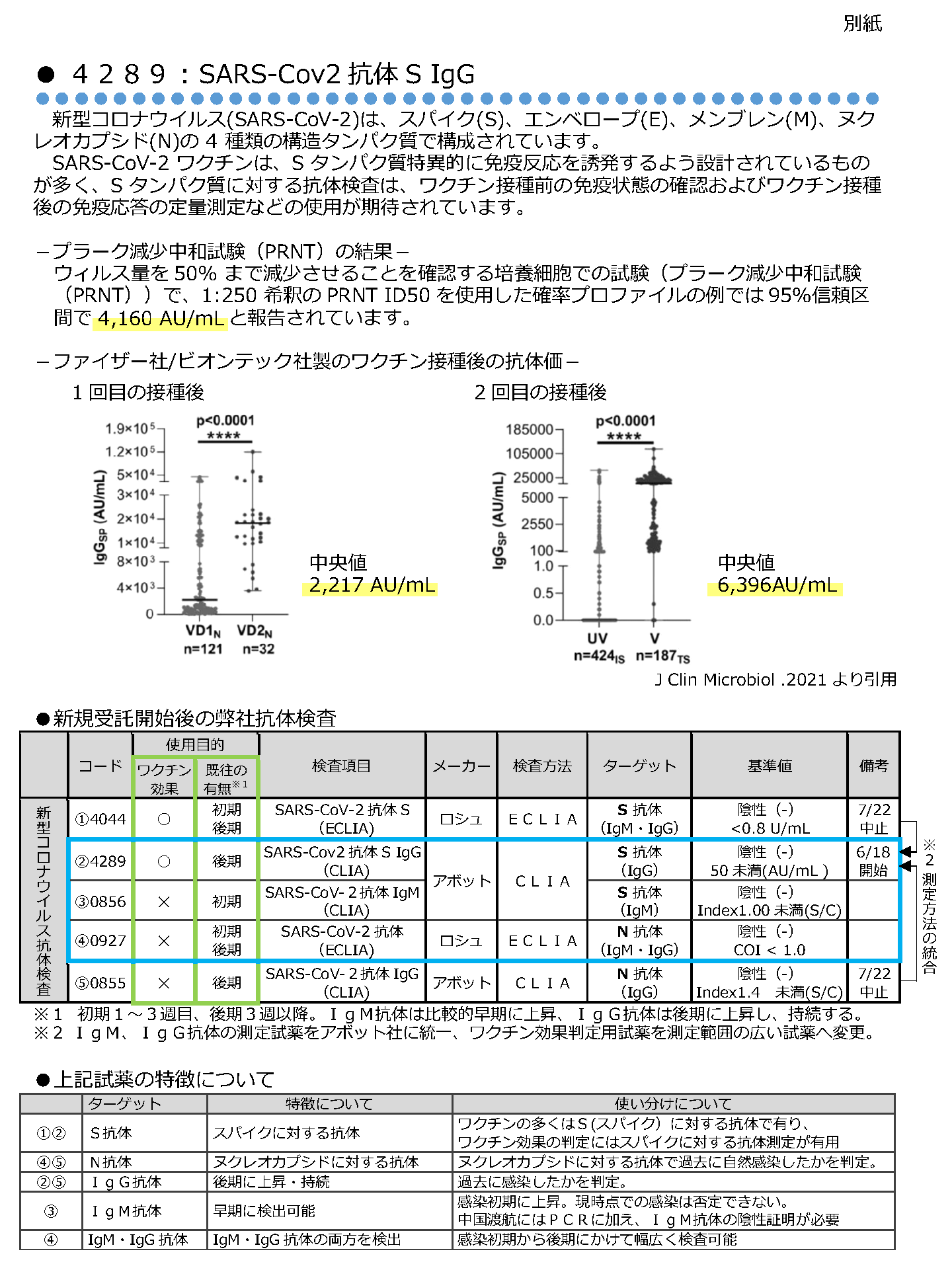
4289 : SARS-Cov2抗体S IgG
SARS-CoV-2 ワクチンは、S タンパク質特異的に免疫反応を誘発するよう設計されているものが多く、S タンパク質に対する抗体検査は、ワクチン接種前の免疫状態の確認およびワクチン接種後の免疫応答の定量測定などの使用が期待されています。
-プラーク減少中和試験(PRNT)の結果-
ウィルス量を50% まで減少させることを確認する培養細胞での試験(プラーク減少中和試験 (PRNT))で、1:250 希釈のPRNT ID50を使用した確率プロファイルの例では95%信頼区間で4,160 AU/mLと報告されています。
-ファイザー社/ビオンテック社製のワクチン接種後の抗体価-
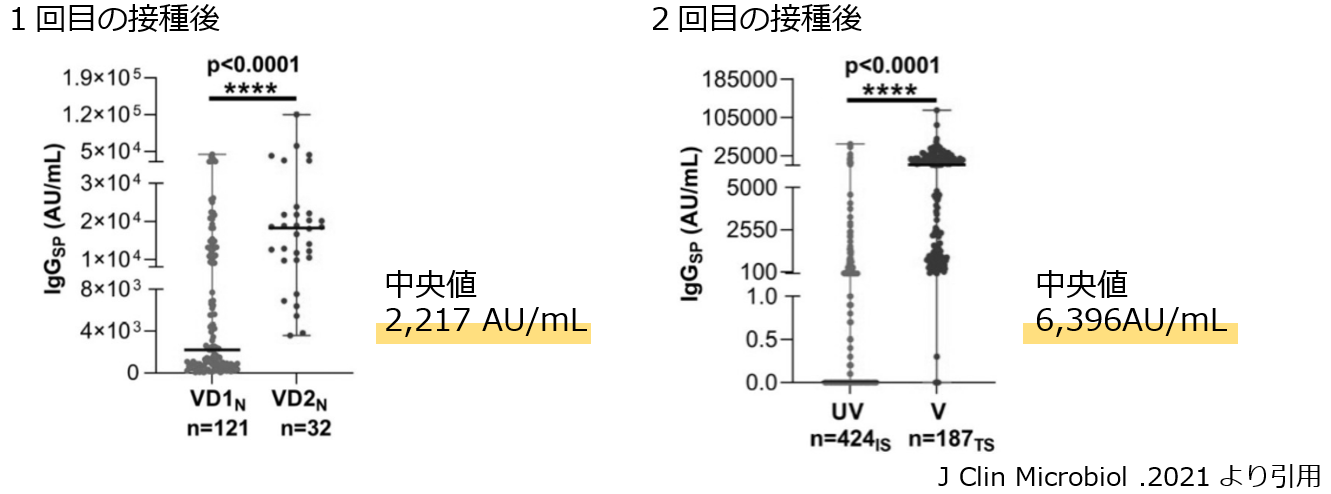
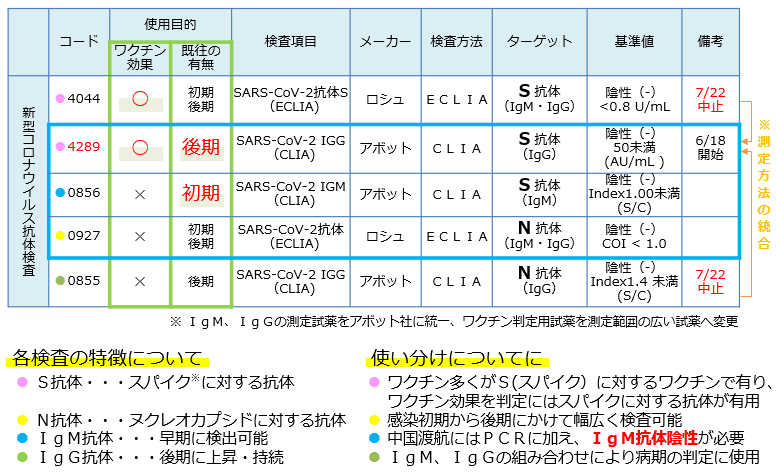
●新規受託開始後の弊社抗体検査
タイトルをクリックをすると展開されます
NEWS(変異株スクリーニング検査受託開始)-2021年4月30日-
■新型コロナウイルス変異株とは → 変異株基礎
NR33004新規
2021年4月
新型コロナウイルス変異株
スクリーニング検査の報告について
謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを賜り
厚くお礼申し上げます。
新型コロナウイルス感染拡大は衰えることはなく、変異株による感染も世界的に増加し
てます。弊社では、新型コロナウイルス関連検査の需要の急速な増加に応えるべく、段階
的に検査受託体制の強化および検査設備の拡充を図ってまいりました。
弊社では、PCR検査を行い陽性となったものについて厚生労働省および国立感染症研
究所からの依頼に基づき、変異株のスクリーニング検査を行政検査として実施してまいり
ましたが、結果についてはご施設様に直接お返しはしていませんでした。このたび、昨今
の感染状況や医療提供体制状況に鑑み、検査させていただきました結果について各ご施設
様にご報告させていただく事となりましたのでご案内申し上げます。
謹白
記
■実施内容及び実施日
|
コード |
検査項目 |
保存方法 |
所要日数 |
検査方法 |
基準値 |
|
4266 |
SARS-CoV-2 N501Y検査※1 |
冷蔵 |
2~3 |
PCR |
野生型 |
※1 本検査は、弊社にて下記対象検査項目をご依頼いただき、検査結果が陽性と確定したものを対象
としています。追加対象項目の結果が陽性と確定した時点で、変異株に共通で認められるN501Y
変異についてのスクリーニング検査を実施させていただきます。行政検査として実施いたします
ので追加料金等は発生いたしません。
|
コード |
検査項目 |
採取量(mL) |
容器※2 |
保存 |
所要 |
実施料 |
検査方法 |
基準値 |
|
0987 |
新型コロナウイルスRNA定性 |
鼻咽頭・鼻腔 |
P1 |
冷蔵 |
2※3 |
1800 |
PCR |
陰性 |
|
喀痰 2.0 |
P1又はL1 |
※2 本検査はPCRメディア等、グアニジンを含むウイルス不活化剤入り容器では、検査結果に影響
を与える(偽陰性となる)ため受託できません。上記指定容器(P1、L1)にてご提出ください。
※3 FAXでのご報告は、再検査を含め、翌朝、変異株スクリーニング検査の結果は翌夕となりますが、
検査キャパシティを大幅に超える受託があった場合、上記報告日数より遅延する可能性があります。
タイトルをクリックをすると展開されます
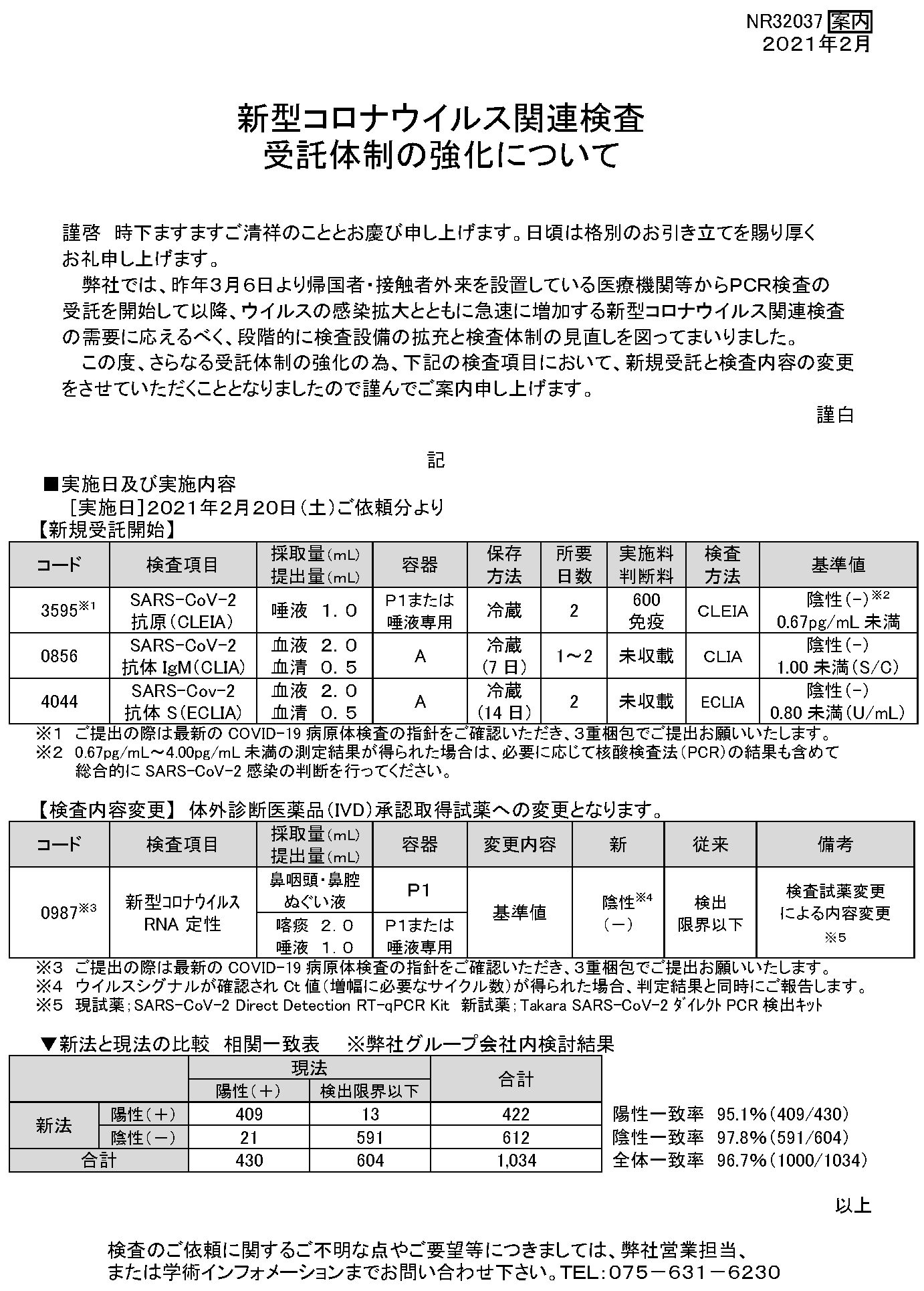
NEWS(新型コロナ関連検査受託体制の強化)-2021年2月17日-
タイトルをクリックをすると展開されます
NEWS(1月連休中の新型コロナウイルス検査受託について)-2020年12月16日-
|
|
|
|
|
|
|
|
検査有無 |
〇 |
〇 |
× |
〇 |
〇 |
〇検査します ×検査しません
タイトルをクリックをすると展開されます
NEWS(年末年始の新型コロナウイルス検査受託について)-2020年11月20日-
| 受付曰 |
検査 |
検査対象 |
FAX |
報告書 |
||
| 12/28 |
月 |
〇 |
12/28搬入分 |
翌朝 |
1/5 |
|
| 12/29 |
火 |
〇 |
12/29搬入分 |
翌朝 |
1/5 |
|
| 12/30 |
水 |
× |
※ |
弊社、配送の一部を外部委託させていただいております。 |
1/6 |
|
| 12/31 |
木 |
〇 |
翌朝 |
|||
| 1/1 |
金 |
× |
||||
| 1/2 |
土 |
〇 |
翌朝 |
|||
| 1/3 |
日 |
× |
|
|||
| 1/4 |
月 |
〇 |
翌朝 |
|||
| 1/5 |
火 |
〇 |
1/5搬入分 |
翌朝 |
1/7 |
|
〇検査します ×検査しません
タイトルをクリックをすると展開されます
NEWS(ドイツの空港における新型コロナウイルス検査について)-2020年11月10日-
ドイツの空港における新型コロナウイルス検査への
高感度抗原検査試薬・検査機器の供給について
タイトルをクリックをすると展開されます
NEWS(検査体制を拡充し、「最短2時間」での陰性証明書発行が可能に)-2020年11月9日-
海外渡航者向け唾液PCR 検査
「羽田空港で最短2 時間」で証明書発行可能に
【PCR 検査予約から証明書受領までの流れ】
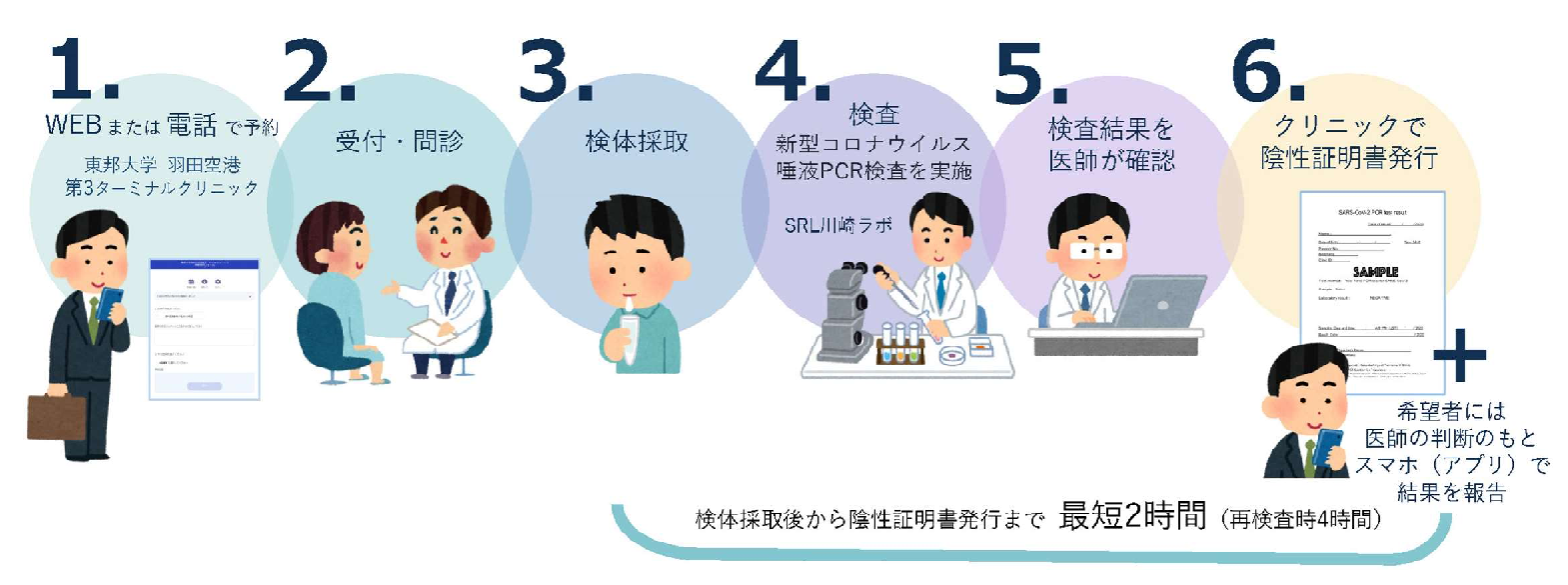
◇ ◇ 東邦大学羽田空港第3ターミナルクリニック ◇ ◇
〇検査を受けることができる対象者(下記全ての条件を満たす方)
・健康な方
・海外渡航のために新型コロナウイルスのPCR 検査が必要な方
・有効期限内のパスポートを有していること
・事前予約された方
〇実施時間
〇検査内容
〇料金
こちらをクリック → “ターミナルクリニック”
こちらをクリック → “唾液PCR 検査について”
以上
<お問い合わせ先>
東邦大学医療センター大森病院事務部総務課
〒143-8541 大田区大森西6-11-1
TEL: 03-3762-4151 9:00-17:30(土日祝除く)
E-mail: somu.omori@jim.toho-u.ac.jp URL: https://www.omori.med.toho-u.ac.jp/
日本空港ビルデング株式会社広報・ブランド戦略室
〒144-0041 大田区羽田空港3-3-2 第1 ターミナルビル
TEL: 03-5757-8030 9:00-17:30(土日祝除く)
URL: https://www.tokyo-airport-bldg.co.jp/company/
東京国際空港ターミナル株式会社
〒144-0041 大田区羽田空港2-6-5
TEL: 03-6428-5901 9:00-17:30(土日祝除く)
E-mail: tiat-kouhou@tiat.co.jp URL: https://www.tiat.co.jp/
H.U.グループホールディングス株式会社コーポレートコミュニケーション部広報課
〒163-0408 新宿区西新宿2-1-1 新宿三井ビルディング
TEL: 03-6279-0884
E-mail: pr@hugp.com URL: https://www.hugp.com/
タイトルをクリックをすると展開されます
NEWS(11月連休中の新型コロナウイルス検査受託について)-2020年10月16日-
|
受付日 |
11/20(金) |
11/21(土) |
11/22(日) |
11/23(月) |
11/24(火) |
|
検査有無 |
〇 |
〇 |
× |
〇 |
〇 |
〇検査します ×検査しません
タイトルをクリックをすると展開されます
NEWS(新型コロナ抗原検査で前鼻腔での検査が追加承認)-2020年10月2日-
■ 陽性一致率等、関連データはこちら → ![]()
【参考:高感度抗原検査および迅速抗原検査の検体種別※1】
検査の対象者 |
核酸検出検査(PCR等) |
迅速(定量)抗原検査 |
迅速(定性)抗原検査 |
|||||||
| 鼻咽頭 |
鼻腔 |
唾液 |
鼻咽頭 |
鼻腔 |
唾液 |
鼻咽頭 |
鼻腔 |
唾液 |
||
| 有症状者 (症状消退者含む) |
発症から 9日目以内 |
〇 |
〇 |
〇 |
〇 |
〇 |
〇 |
〇※2 |
〇※2 |
☓ |
| 発症から 10日目以降 |
〇 |
〇 |
-※4 |
〇 |
〇 |
-※4 |
△※3 |
△※3 |
☓ |
|
| 無症状者 |
〇 |
-※4 |
〇 |
〇 |
-※4 |
〇 |
-※4 |
-※4 |
☓ |
|
※1 第 47 回厚生科学審議会感染症部会 参考資料 2 「新型コロナウイルス感染症病原体検査の指針」参照
※2 発症 2 日目から 9 日目以内の有症状者の確定診断に用いられる
※3 使用可能だが、陰性の場合は鼻咽頭 PCR 検査を行う必要あり
※4 推奨されない
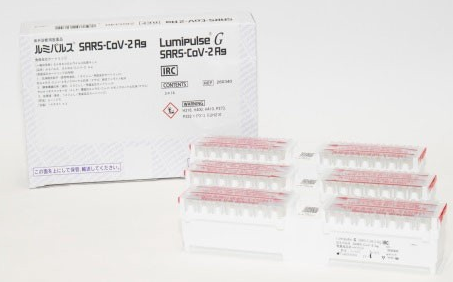
【参考:製品情報】
| 製品名 |
ルミパルス SARS-CoV-2 Ag |
エスプライン SARS-CoV-2 |
| 製造販売 承認取得日 |
2020年6月19日 |
2020年5月13日 |
| 対象機器 |
ルミパルスG600 ルミパルスG1200 |
機器不要 |
| 検査時間 |
約30分 |
30分以内 陽性判定:約10~30分 陰性判定:30分 |
| 製品イメージ |
 |
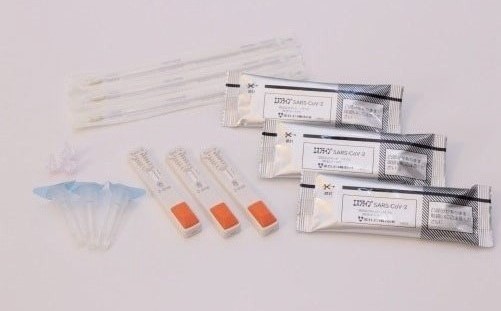 |
タイトルをクリックをすると展開されます
NEWS(海外渡航者新型コロナウイルス検査センター(TeCOT)を開設について)-2020年9月7日-
タイトルをクリックをすると展開されます
NEWS(9月連休中の新型コロナウイルス検査受託について)-2020年9月2日-
|
受付日 |
9/19(土) |
9/20(日) |
9/21(月) |
9/22(火) |
9/23(水) |
|
検査有無 |
〇 |
× |
〇 |
× |
× |
〇検査します ×検査しません
タイトルをクリックをすると展開されます
NEWS(新型コロナウイルス陰性証明書について)-2020年8月12日-
■証明書(日本語)WORD版のダウンロードはこちら →  (タカラバイオ社製)
(タカラバイオ社製)
■証明書(日本語)WORD版のダウンロードはこちら →  (ロシュ社製)
(ロシュ社製)
■証明書( 英語 ) WORD版のダウンロードはこちら →  (タカラバイオ社製)
(タカラバイオ社製)
■証明書( 英語 ) WORD版のダウンロードはこちら →  (ロシュ社製)
(ロシュ社製)
タイトルをクリックをすると展開されます
NEWS(環境中の新型コロナウイルス拭き取り検査について)-2020年8月3日-
タイトルをクリックをすると展開されます
NEWS(SARS-CoV-2及びインフルエンザの迅速抗原検査について)-2020年7月27日-
タイトルをクリックをすると展開されます
NEWS(SARS-COV-2抗体所要日数短縮のお知らせ)-2020年7月22日-
■PDFのダウンロードはこちら → ![]()
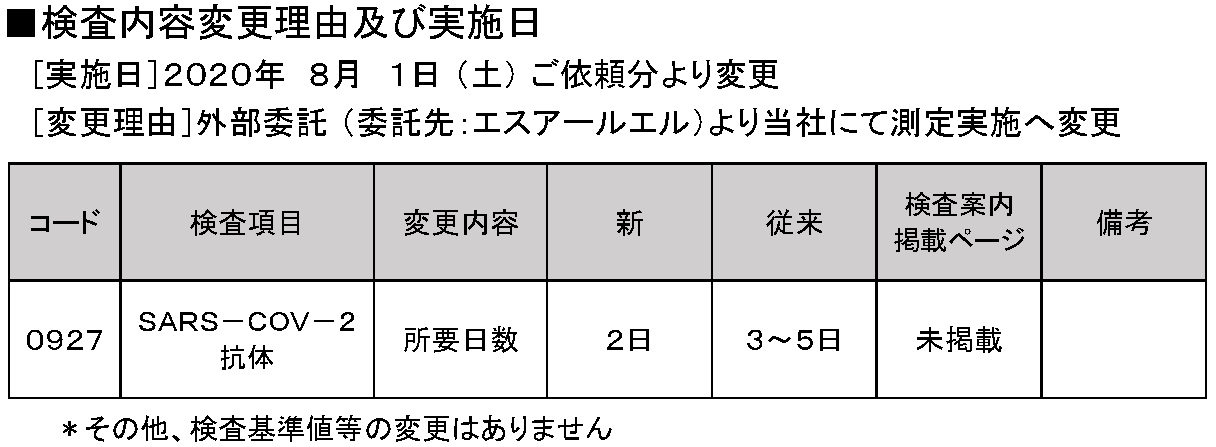
■検査内容変更理由及び実施日
| コード | 検査項目 | 変更内容 | 新 | 従来 | 検査案内 掲載ページ |
備考 |
| 0927 | SARS-COV-2 抗体 |
所要日数 | 2日 | 3~5日 | 未掲載 |
タイトルをクリックをすると展開されます
NEWS(新型コロナウイルスPCR検査試薬変更のお知らせ)-2020年7月21日-
| コード | 検査項目 | 変更内容 | 新 | 従来 | 検査案内 掲載ページ |
備考 |
| 0987 | 新型コロナウイルス RNA定性 |
報告 方法 |
検出限界以下 | 陰性(-) | 未掲載 | |
| 陽性 | 陽性(+) |
*尚、上記試薬変更に伴い検査体制が整い8月8日(土)より土曜日の検査を開始させていただきます。
| 現法 | ||||
| 陽性 | 陰性 | 合計 | ||
| 新法 | 陽性 | 11 | 0 | 11 |
| 陰性 | 0 | 11 | 11 | |
| 合計 | 11 | 11 | 22 | |
タイトルをクリックをすると展開されます
NEWS(新型コロナウイルス(SARS-CoV-2)PCR 検査体制について)-2020年7月20日-
検査項目【0987】新型コロナウイルスRNA 定性は、上記期間中は、2020 年7 月24 日(金)に平日と同様に検査を実施します。
タイトルをクリックをすると展開されます
NEWS(無症状者の唾液PCR検査・抗原定量検査が可能に)-2020年7月17日-
*無症候性感染には抗体検査が有効です。PCR検査との併用をおすすめします。
タイトルをクリックをすると展開されます
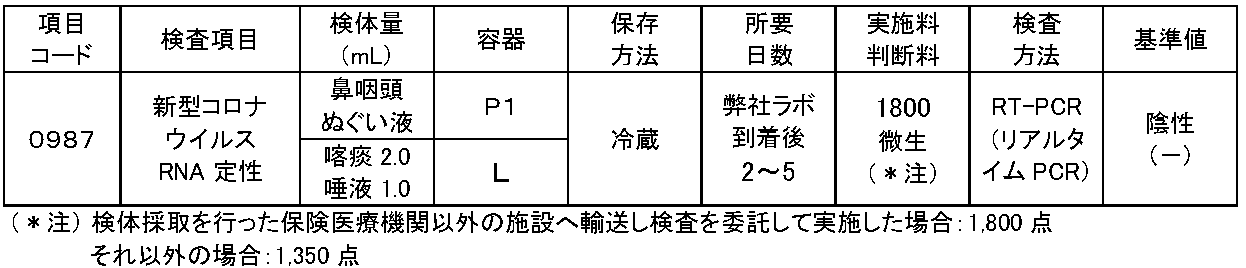
NEWS(唾液を用いたコロナウイルスPCR検査について)-2020年6月4日-
| 項目 コード |
検査項目 | 検体量 (mL) |
容器 | 保存 方法 |
所要 日数 |
実施料 判断料 |
検査 方法 |
基準値 |
| 0987 | 新型コロナ ウイルス RNA定性 |
鼻咽頭 ぬぐい液 |
P1 | 冷蔵 | 弊社ラボ 到着後 2~5 |
1800 微生 (*注) |
RT-PCR (リアルタイムPCR) |
陰性 (-) |
| 喀痰2.0 唾液1.0 |
L |
(*注) 弊社へ検査を委託して実施した場合:1,800 点、自施設で実施した場合:1,350 点
■保険適応に関する注意点PDF → ![]()
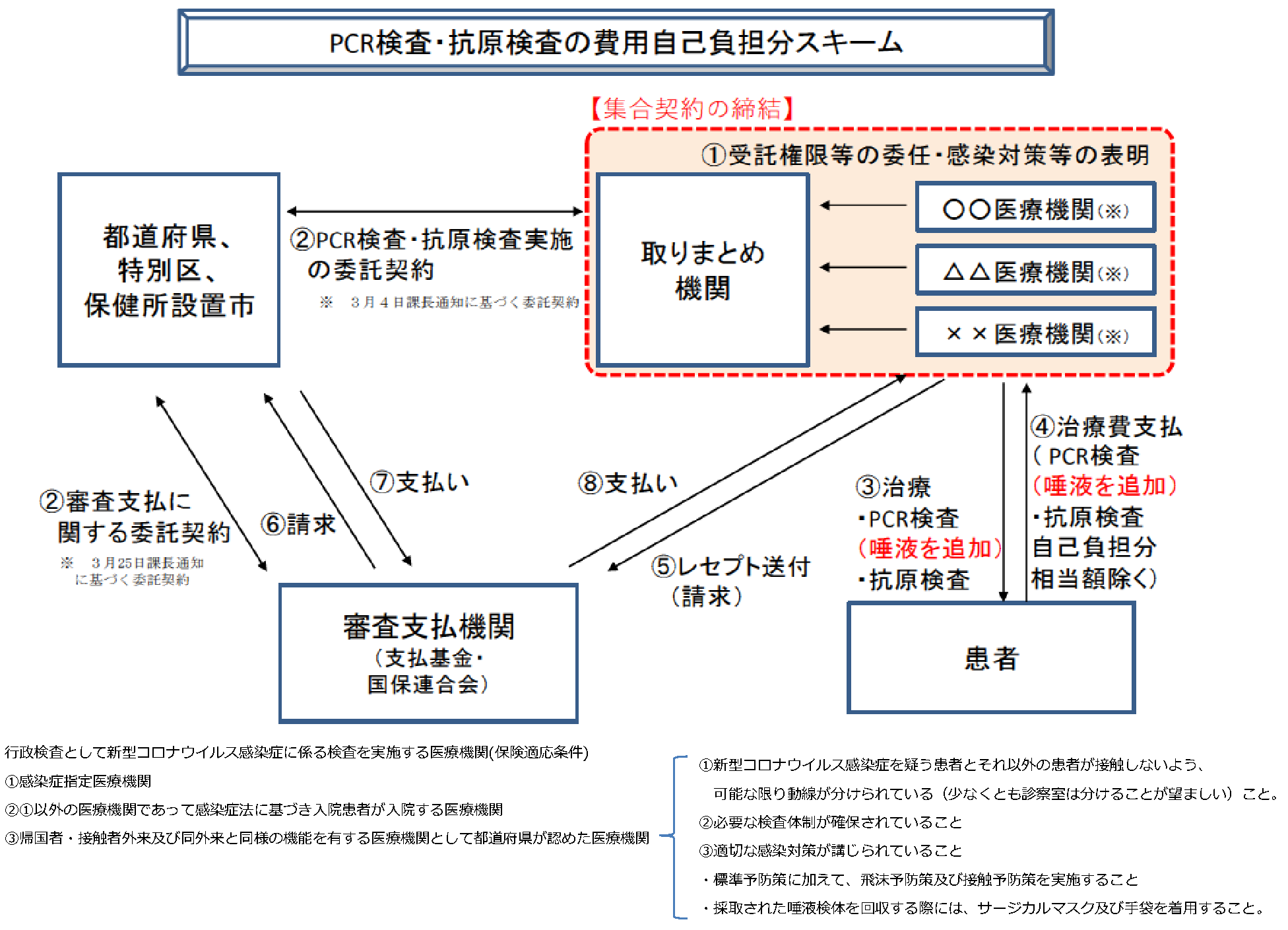
![]() 保険適応内での検査には都道府県への申請が必要です。
保険適応内での検査には都道府県への申請が必要です。
![]() 検体採取方法について
検体採取方法について
■検体採取に関する注意点PDF → ![]()

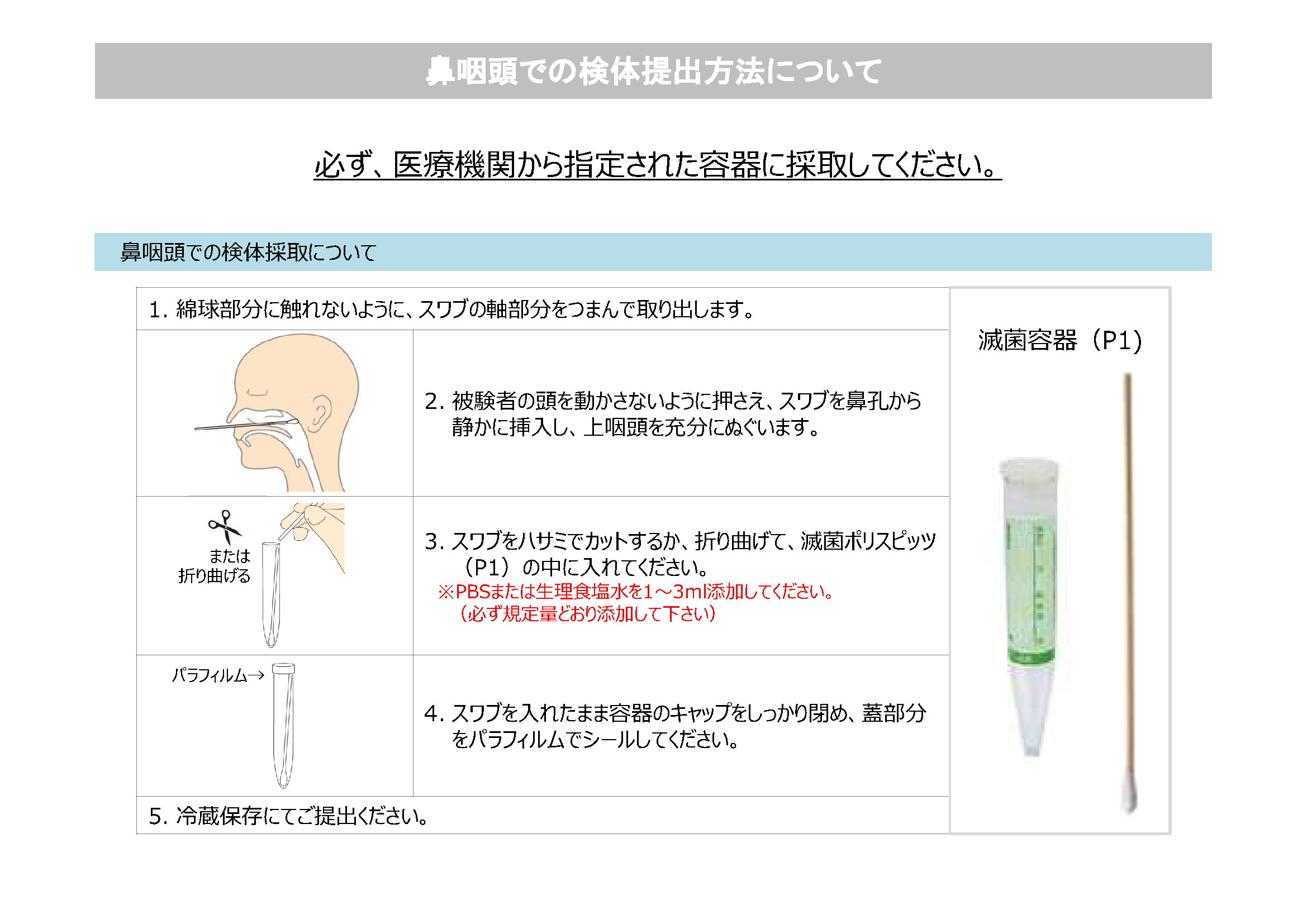
![]() 検体提出方法について
検体提出方法について
〇搬送方法(弊社自社便をご利用の場合)
お近くの営業所にご連絡ください
■弊社自社便で搬送される場合の提出方法PDF → ![]()
〇搬送方法(ゆうパックを利用の場合)
お近くに弊社営業所がない場合、ゆうパックでも検査を受け付けております
■郵送を利用される場合の提出方法PDF → ![]()
*弊社自社便で搬送される場合、ゆうパックを利用される場合、ともに検体のご提出される際は、事前予約が必要です。
タイトルをクリックをすると展開されます
NEWS(新型コロナウイルス抗体検査受託開始のお知らせ)-2020年6月1日-
タイトルをクリックをすると展開されます
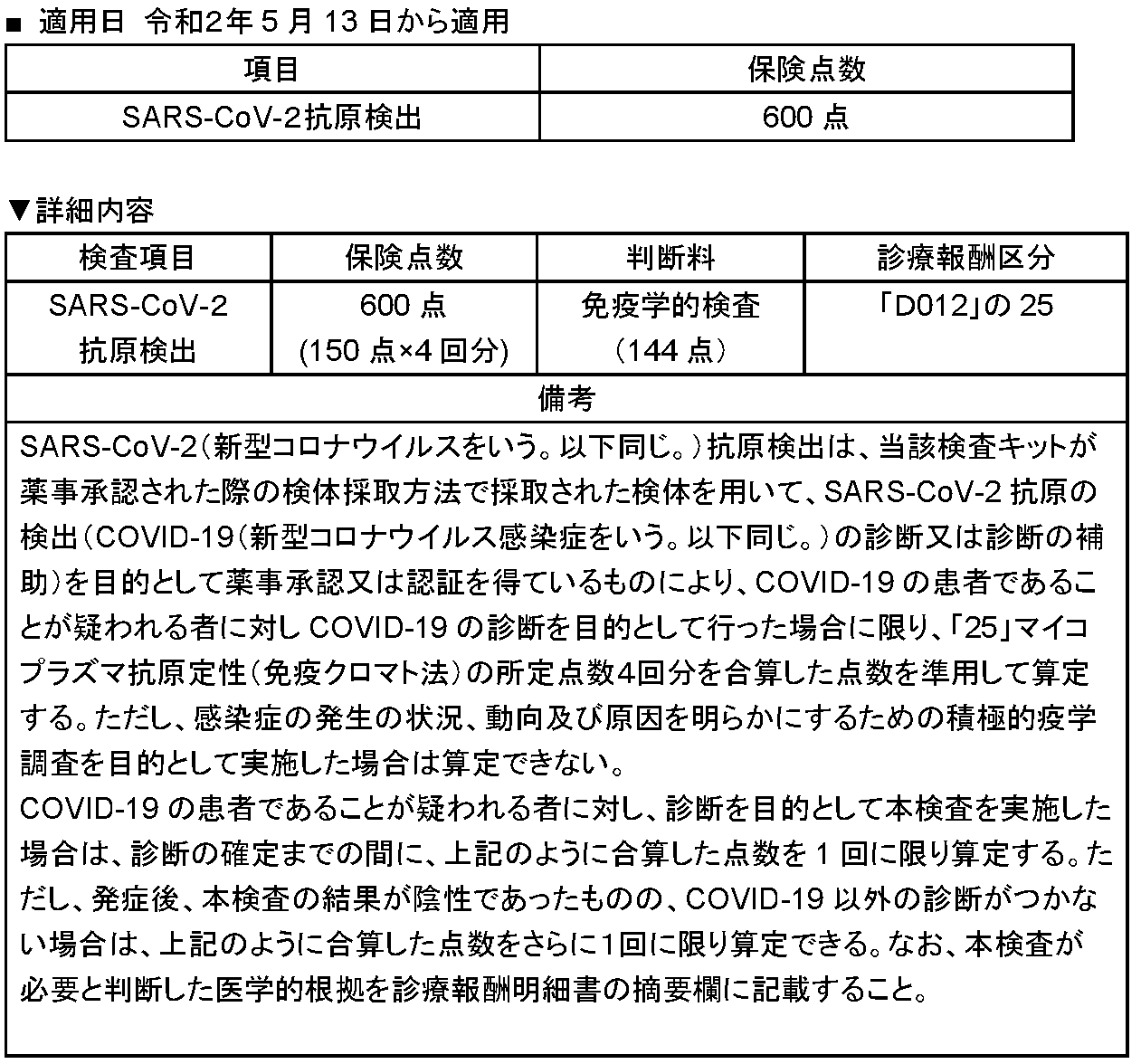
NEWS(新型コロナウイルス抗原検査実施料新設のお知らせ)-2020年5月13日-
|
項目 |
保険点数 |
|
SARS-CoV-2抗原検出 |
600点 |
▼詳細内容
|
検査項目 |
保険点数 |
判断料 |
診療報酬区分 |
|
SARS-CoV-2 抗原検出 |
600点 (150点×4回分) |
免疫学的検査 (144点) |
「D012」の25 |
|
備考 |
|||
|
SARS-CoV-2(新型コロナウイルスをいう。以下同じ。)抗原検出は、当該検査キットが薬事承認された際の検体採取方法で採取された検体を用いて、SARS-CoV-2抗原の検出(COVID-19(新型コロナウイルス感染症をいう。以下同じ。)の診断又は診断の補助)を目的として薬事承認又は認証を得ているものにより、COVID-19の患者であることが疑われる者に対しCOVID-19の診断を目的として行った場合に限り、「25」マイコプラズマ抗原定性(免疫クロマト法)の所定点数4回分を合算した点数を準用して算定する。ただし、感染症の発生の状況、動向及び原因を明らかにするための積極的疫学調査を目的として実施した場合は算定できない。 |
|||


タイトルをクリックをすると展開されます
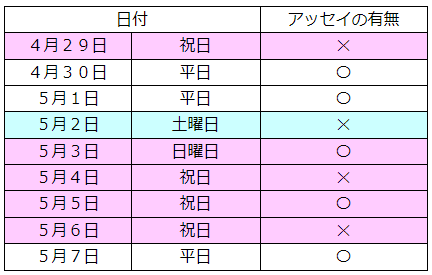
NEWS(GW中の新型コロナウイルス検査受託について)-2020年4月16日-
|
日付 |
アッセイの有無 |
|
|
4月29日 |
祝日 |
✕ |
|
4月30日 |
平日 |
〇 |
|
5月1日 |
平日 |
〇 |
|
5月2日 |
土曜日 |
✕ |
|
5月3日 |
日曜日 |
〇 |
|
5月4日 |
祝日 |
✕ |
|
5月5日 |
祝日 |
〇 |
|
5月6日 |
祝日 |
✕ |
|
5月7日 |
平日 |
〇 |
タイトルをクリックをすると展開されます
NEWS(重要なお知らせ)-2020年4月1日-
タイトルをクリックをすると展開されます
NEWS(新型コロナウイルスの受託開始のお知らせ)-2020年3月6日-
尚、2020年 3月 6日(金)時点での受託可能な施設として、各都道府県等が認めた医療機関であり、「感染症法第15条に基づく調査に関する事務契約書」を各都道府県と締結された医療機関とさせていただきます。
|
項目 |
検査項目 |
検体量 |
容器 |
保存 |
所要 |
実施料 |
検査 |
基準値 |
備考 |
|
987 |
新型コロナ |
鼻咽頭 |
P1 |
冷蔵 |
弊社ラボ 到着後 2~5 |
1800 |
RT-PCR |
陰性 |
検体採取 |
|
喀痰 |
L |
地図中のアイコンをクリックすると住所と電話番号が表示されます。
日々、医療業務に携わる先生方のために、日本臨床が検査を
- ページの選択 -
- 2021年12月27日から2021年1月4日における新型コロナウイルスPCR検査体制についてお知らせします。
- 2021年8月13日から2021年8月16日における新型コロナウイルスPCR検査体制についてお知らせします。
- オリンピック閉会式前後における新型コロナウイルスPCR検査体制についてお知らせします。
- オリンピック開会式前後における新型コロナウイルスPCR検査体制についてお知らせします。
- 2021年1月10日・11日の連休における新型コロナウイルスPCR検査体制についてお知らせします。
- 検査項目【0987】新型コロナウイルス RNA 定性は、2021 年 1 月 11 日(月)の15:00までに所定場所(本社コロナ検査検体搬入場所)に搬入された検体について、1月10日(日)搬入分と合わせて、1月11日に検査を行います(1 月 10 日は検査を行いません)。
- 至急FAX 分については1月11日(月)検査終了後に報告します。報告書は1月13日(水)の報告となります。
- 2020年12月28日から2021年1月5日における新型コロナウイルスPCR検査体制についてお知らせします。
- ドイツの空港における新型コロナウイルス検査への高感度抗原検査試薬・検査機器の供給について
- 海外渡航者向け唾液PCR検査証明書発行「羽田空港で最短2時間」に
- 東邦大学、日本空港ビルデング株式会社、東京国際空港ターミナル株式会社、H.U.グループホールディングス株式会社は、東邦大学羽田空港第3ターミナルクリニックにて実施中の唾液PCR検査について、検査体制を拡充し、11月9日より検体採取後「最短2時間」での陰性証明書発行が可能になります。
- また、本クリニックのホームページにおいてご提供しているオンライン予約に加え、スマートフォンのアプリに検査結果を通知するサービスを開始します。
- これにより羽田空港における海外渡航者向けPCR 検査の利便性を高め、空の旅を通じた国際間の往来再開に向けて貢献してまいります。
- ※H.U.グループホールディングス株式会社は、傘下のグループ会社が本クリニックよりPCR 検査を受託するとともに、検査結果を確認できるPHR アプリ「ウィズウェルネスTM」を提供しています。
- 【ウィズウェルネスについて】
- ~海外渡航者向け唾液PCR 検査~
- 検体採取:全日(土日祝日を含む)
- 午前9:00-11:30、午後13:00-17:30
- 証明書発行:全日(土日祝日を含む)
- 午前9:00-11:30、午後13:00-22:00
- 唾液PCR 検査(RT-PCR)
- 38,500 円(税込)
- (検査料・証明書発行料を含みます。)
- 各種クレジット払い対応
- 詳細は下記のURL よりご確認ください。
- 〇東邦大学羽田空港第3ターミナルC
- 〇海外渡航者向け唾液PCR 検査について
- 先日、経済産業省より渡航先国の要求に応じた新型コロナウイルス陰性検査証明を円滑に取得するための仕組みである海外渡航者新型コロナウイルス検査センター(TeCOT)を開設するとの発表がありましたが、参加される医療機関様の正式登録が始まりました。申請の際には委託先の衛生検査所等の詳細情報が必要となってきます。弊社、必要書類情報は下記リンクよりご確認ください。
- 2020 年9月 20 日・21 日・22 日の連休における新型コロナウイルス PCR 検査体制についてお知らせします。
- 検査項目【0987】新型コロナウイルス RNA 定性は、2020 年 9 月 21 日(月)の15:00 までに弊社に搬入された検体について、9 月 20 日(日)搬入分と合わせて、9 月 21 日に検査を行います(9 月 20 日・22 日は検査を行いません)。至急 FAX 分については 9 月 21 日(月)検査終了後に報告します。報告書は9月 24 日(木)の報告となります。
- 当社のグループ会社で新型コロナウイルスの環境中における拭き取り検査の受託を開始いたしました。
- 当社のグループ会社である株式会社日本食品エコロジー研究所と、みらかヴィータス株式会社は、2020年8月3日より、新型コロナウイルス(SARS-CoV-2)の環境中における拭き取り検査の受託を開始いたしましたのでお知らせいたします。
- 本検査は、医療機関や飲食店・宿泊施設等の法人をサービスの対象として想定しております。ドアノブやテーブル、手すり、エレベーターボタン等、人の手が多く触れる箇所を綿棒により拭き取ることによって検体を採取し、PCR検査を実施します。
- 当社グループは、これまで臨床検査領域で培った検査技術を応用し、環境中の新型コロナウイルスの拭き取り検査を受託することで、人々の暮らしの安全と感染拡大の抑制に貢献してまいります。
- 鼻咽頭拭い液検体1本で新型コロナウイルス抗原とインフルエンザウイルス抗原の迅速検査が可能です。
- 当社のグループ会社である富士レビオ株式会社は、新型コロナウイルス(SARS-CoV-2)抗原の迅速診断キット「エスプライン®SARS-CoV-2」で用いる検体処理液が、インフルエンザウイルス抗原の迅速診断キット「エスプラインインフルエンザA&B-N」においても使用できることを確認しましたのでお知らせいたします。
- 検査を同一の鼻咽頭拭い液検体で行うことが可能となり、検体採取が1回で済むことから、検体採取時における患者さまの負担軽減および医療従事者の感染リスクを低減することに貢献することができるものと考えております。
- この度、SARS-COV-2抗体の検査項目につきまして検査所要日数を変更いたします
- 感染の拡大がほぼ終息したと思われていた新型コロナウイルスが再度、流行の兆しを見せており、弊社でもPCR検査受託数が急増しております。試薬の安定受給と検査受託数拡大の為、試薬を変更いたします。
- 尚、本試薬は国立感染症研究所「病原体検出マニュアル 2019-nCoV Ver.2.6」に記載のキット間の比較検討に基づき、国立感染症研究所の方法と同等であると評価された試薬です。
- 厚生労働省は2020年7月17日、新型コロナウイルス感染症の診断に用いるPCR検査および抗原定量検査について、唾液検体を用いた検査の対象を空港検疫の対象者、濃厚接触者などを含む無症状者にも拡大する方針を示しました。
- 出典:厚生労働省「無症状者の唾液を用いたPCR検査等について」
- ~新型コロナウイルス検査の使い分け~
- このたび、唾液を用いた新型コロナウイルス PCR 検査の受託を開始いたしましたのでご案内いたします。
- 弊社ではコロナ禍の早急な終息の為、保険適応外でのPCR 検査も積極的に受託することといたしました。
- 新型コロナウイルスに感染した患者様の早期回復と一刻も早い事態の鎮静化を心よりお祈り申し上げます。
- 「保医発0513第1号」により下記の検査項目に検査実施料が新設されましたので、ご案内いたします。
- *簡易キットについては弊社でも販売しております。お近くの営業所へお申し付けください。
- GW中の新型コロナウイルス検査受託についてアッセイ日が決定しましたのでお知らせいたします。
- GW期間中は19:00までに搬入されたものを当日受付とさせていただきます。
- (ゆうパックの受け取りは土日祝でも行いますが、アッセイは上記スケジュールとなります。)
- また、報告は過誤防止のため、通常通りの運用とさせていただきたいと考えています。
- 新型コロナウイルスについて現在、検体量が増えており、当初、翌日には報告させていただいていましたが、報告に2~5日の時間をいただいております。ご利用の先生方には大変ご迷惑をおかけすることと存じますが、何卒ご了承賜りますよう宜しくお願い申し上げます。
- 株式会社日本医学臨床検査研究所は、新型コロナウイルス(SARS-CoV-2)の検査を3月6日より臨床検査として受託することとなりましたのでお知らせいたします。
- 弊社は、厚生労働省および国立感染症研究所からの依頼に基づき、これまでも行政検査として本検査を受託してまいりましたが、このたび、帰国者・接触者外来を設置している医療機関等における検査が3月6日に保険適用されることを受け、臨床検査としての受託を開始するものです。
(現在の所要日数)
〇*FAX報告は弊社検査室到着の
翌朝~翌々日 です。
*検査キャパを大幅に超える受託があった場合、上記報告日数より遅延する可能性があります。
提出方法等はこちら→詳細表示
☆☆☆トピックス☆☆☆
■コロナ検査使い分け(病原体検査の指針)
リンクはこちら → “使い分け方”
■新型コロナ消毒・除菌方法について
リンクはこちら → “消毒・除菌方法”
■ 日本からの渡航・各国入国制限措置等
リンクはこちら → “制限措置等”
~LINE公式アカウントを開設いたしました~
新型コロナウイルス情報、弊社からのお知らせ、最新トピックス、採用情報等の情報をスマホで確認いただけます。
またAI機能を利用した検査項目検索など様々な機能が搭載されています。検査項目案内の代わりにご使用ください。
※下記、画像をクリックしてください。
▼ご提出方法
▼保険点数詳細内容
SARS-CoV-2核酸検出

SARS-CoV-2・インフルエンザ核酸同時検出
SARS-CoV-2抗原検出(定性)
SARS-CoV-2・インフルエンザ抗原同時検出(定性)

SARS-CoV-2抗原検出(定量)
タイトルをクリックをすると展開されます
PCR検査実施料に関するお知らせ
-2022年3月28日-
-2022年3月28日-
タイトルをクリックをすると展開されます
年末年始の新型コロナ検査受託について
-2021年12月1日-
-2021年12月1日-
タイトルをクリックをすると展開されます
変異株スクリーニング検査受託中止について
-2021年10月15日-
-2021年10月15日-
表示拡大はこちら → “お知らせ”
タイトルをクリックをすると展開されます
お盆期間中の新型コロナ検査受託について
-2021年7月26日-
-2021年7月26日-
タイトルをクリックをすると展開されます
SARS-CoV2抗体等の項目名称変更
-2021年7月20日-
-2021年7月20日-
表示拡大はこちら → “お知らせ”
タイトルをクリックをすると展開されます
五輪閉会式前後の検査受託について
-2021年7月12日-
-2021年7月12日-
タイトルをクリックをすると展開されます
五輪開会式前後の検査受託について
-2021年7月1日
-2021年7月1日
タイトルをクリックをすると展開されます
SARS-Cov2抗体S IgG 受託開始のお知らせ
-2021年6月7日-
-2021年6月7日-
表示拡大はこちら → “お知らせ”
タイトルをクリックをすると展開されます
変異株スクリーニング検査受託開始
-2021年4月30日-
-2021年4月30日-
SARS-COV2変異株とは → 変異株
NR33004新規
2021年4月
新型コロナウイルス変異株
スクリーニング検査の報告について
謹啓 時下ますますご清祥のこととお慶び申し上げます。日頃は格別のお引き立てを賜り厚くお礼申し上げます。
弊社では、PCR検査を行い陽性となったものについて厚生労働省および国立感染症研究所からの依頼に基づき、変異株のスクリーニング検査を行政検査として実施してまいりましたが、結果についてはご施設様に直接お返しはしていませんでした。このたび、昨今の感染状況や医療提供体制状況に鑑み、検査させていただきました結果について各ご施設様にご報告させていただく事となりましたのでご案内申し上げます。
謹白
記
■実施内容及び実施日
[実施日]2021年5月 8日(土)ご依頼分より
|
コード |
検査項目 |
保存方法 |
所要日数 |
検査方法 |
基準値 |
|
4266 |
SARS-CoV-2 |
冷蔵 |
2~3 |
PCR |
野生型 |
※1本検査は、弊社にて下記対象検査項目をご依頼いただき、検査結果が陽性と確定したものを対象としています。追加対象項目の結果が陽性と確定した時点で、変異株に共通で認められるN501Y変異についてのスクリーニング検査を実施させていただきます。行政検査として実施いたしますので追加料金等は発生いたしません。
[変異株スクリーニング検査追加対象項目]
|
コード |
検査項目 |
採取量(mL) |
容器※2 |
保存 |
所要 |
実施料 |
検査方法 |
基準値 |
|
0987 |
新型コロナウイルス |
鼻咽頭・鼻腔 |
P1 |
冷蔵 |
2※3 |
1800 |
PCR |
陰性 |
|
喀痰 2.0 |
P1又はL1 |
※2本検査はPCRメディア等、グアニジンを含むウイルス不活化剤入り容器では、検査結果に影響を与える(偽陰性となる)ため受託できません。上記指定容器(P1、L1)にてご提出ください。
※3FAXでのご報告は、再検査を含め、翌朝、変異株スクリーニング検査の結果は翌夕となりますが、検査キャパシティを大幅に超える受託があった場合、上記報告日数より遅延する可能性があります。
タイトルをクリックをすると展開されます
新型コロナ関連検査受託体制の強化
-2021年2月17日-
-2021年2月17日-
タイトルをクリックをすると展開されます
1月連休中の新型コロナ検査受託について
-2020年12月16日-
-2020年12月16日-

タイトルをクリックをすると展開されます
年末年始の新型コロナ検査受託について
-2020年11月20日-
-2020年11月20日-
タイトルをクリックをすると展開されます
ドイツの空港における検査について
-2020年11月10日-
-2020年11月10日-
ドイツの空港における
SARS-COV-2検査への高感度抗原
検査試薬・検査機器供給について
詳細確認はこちら → “詳細情報”
弊社グループ会社である富士レビオ・ホールディングス株式会社傘下の Fujirebio Europe N.V.(ベルギー)は、Centogene社(ドイツ:欧州で遺伝子関連検査ビジネスを手掛ける)との間で、全自動化学発光酵素免疫測定システム「ルミパルス® G1200」および高感度抗原検査試薬「ルミパルス SARS-CoV-2Ag」を供給することで合意いたしました。
Centogene社は、ドイツの主要空港において新型コロナウイルスのPCR検査を旅行者および空港勤務者に対して実施しております。この度、Centogene社とルフトハンザグループが提携したことに伴い、2020年11月12日よりハンブルク空港を出発するルフトハンザドイツ航空の指定されたフライトに搭乗する乗客は、本試薬を用いた高感度抗原検査を受けることができるようになります。
今後、Centogene社がハンブルク空港以外で展開する新型コロナウイルス検査においても高感度抗原検査が採用される予定です。
タイトルをクリックをすると展開されます
空港で最短2時間で陰性証明書発行が可能に
-2020年11月9日-
-2020年11月9日-
詳細の確認はこちら → “詳細情報”
海外渡航者向け
唾液PCR検査証明書発行
「羽田空港で最短2時間」に
【PCR検査予約から証明書受領の流れ】

詳細はこちら → “詳細情報”
◇東邦大学羽田空港
第3ターミナルクリニック◇
〇検査を受けることができる対象者
(下記全ての条件を満たす方)
・健康な方
・海外渡航のためにPCR検査が必要な方
・有効期限内のパスポートを保有
・事前予約された方
〇実施時間
〇検査内容
〇料金
<お問い合わせ先>
東邦大学医療C大森病院事務部総務課
〒143-8541 大田区大森西6-11-1
TEL: 03-3762-4151
9:00-17:30(土日祝除く)
E-mail: somu.omori@jim.toho-u.ac.jp
URL: https://www.omori.med.toho-u.ac.jp/
日本空港ビルディング株式会社
広報・ブランド戦略室
〒144-0041
大田区羽田空港3-3-2 第1ターミナルビル
TEL: 03-5757-8030
9:00-17:30(土日祝除く)
URL: https://www.tokyo-airport-bldg.co.jp/company/
東京国際空港ターミナル株式会社
〒144-0041 大田区羽田空港2-6-5
TEL: 03-6428-5901
9:00-17:30(土日祝除く)
E-mail: tiat-kouhou@tiat.co.jp
URL: https://www.tiat.co.jp/
H.U.グループホールディングス株式会社
コーポレートコミュニケーション部
広報課
〒163-0408
新宿区西新宿2-1-1 新宿三井ビルディング
TEL: 03-6279-0884
E-mail: pr@hugp.com
URL: https://www.hugp.com/
タイトルをクリックをすると展開されます
海外渡航者新型コロナ検査センターを開設
-2020年9月7日-
-2020年9月7日-
タイトルをクリックをすると展開されます
9月連休中の新型コロナ検査受託について
-2020年9月2日-
-2020年9月2日-

〇検査します ×検査しません
タイトルをクリックをすると展開されます
環境中の新型コロナ拭き取り検査について
-2020年8月3日-
-2020年8月3日-
PDFはこちら → “お知らせ”
タイトルをクリックをすると展開されます
コロナ及びインフルエンザの迅速抗原検査について
-2020年7月27日-
-2020年7月27日-
PDFはこちら → “お知らせ”
タイトルをクリックをすると展開されます
SARS-COV-2抗体所要日数短縮のお知らせ
-2020年7月22日-
-2020年7月22日-
表示拡大はこちら → “お知らせ”
タイトルをクリックをすると展開されます
新型コロナPCR検査試薬変更のお知らせ
-2020年7月21日-
-2020年7月21日-
表示拡大はこちら → “お知らせ”
タイトルをクリックをすると展開されます
無症状者の唾液PCR検査・抗原定量検査
-2020年7月17日-
-2020年7月17日-


*無症候性感染には抗体検査が有効です。PCR検査との併用をおすすめします。
タイトルをクリックをすると展開されます
唾液を用いた新型コロナPCR検査について
-2020年6月4日-
-2020年6月4日-
■受託開始に関するお知らせPDF
表示拡大はこちら → “お知らせ”
■保険適応に関する注意点PDF
表示拡大はこちら → “保険適応手順”

![]() 保険適応内での検査には都道府県への申請が必要です。
保険適応内での検査には都道府県への申請が必要です。

![]() 検体採取方法について
検体採取方法について
■検体採取に関する注意点PDF
リンクはこちら →“採取注意点”


![]() 検体提出方法について
検体提出方法について
〇搬送方法(弊社自社便をご利用の場合)
お近くの営業所にご連絡ください
■弊社自社便で搬送提出方法
リンクはこちら →“搬送提出方法”
〇搬送方法(ゆうパックを利用の場合)
お近くに弊社営業所がない場合、ゆうパックでも検査を受け付けております
■郵パックでの搬送提出方法
リンクはこちら →“郵送での提出方法”
*弊社自社便で搬送される場合、ゆうパックを利用される場合、ともに検体のご提出される際は、事前予約が必要です。
タイトルをクリックをすると展開されます
新型コロナ抗原検査実施料新設のお知らせ
-2020年5月13日-
-2020年5月13日-
表示拡大はこちら → “お知らせ”
■エスプラインリーフレット
リンクはこちら →“リーフレット”


タイトルをクリックをすると展開されます
GW中の新型コロナ検査受託について
-2020年4月16日-
-2020年4月16日-
タイトルをクリックをすると展開されます
検査受託に関する重要なお知らせ
-2020年4月1日-
-2020年4月1日-
タイトルをクリックをすると展開されます
新型コロナ受託開始のお知らせ
-2020年3月6日-
-2020年3月6日-
尚、2020年 3月 6日(金)時点での受託可能な施設として、各都道府県等が認めた医療機関であり、「感染症法第15条に基づく調査に関する事務契約書」を各都道府県と締結された医療機関とさせていただきます。

■受託開始に関するお知らせPDF
表示拡大はこちら → “お知らせ”
日々、医療業務に携わる先生方のために、
PDFはこちら → “日本臨床LINE”
- ページの選択 -